Cum influențează nutriția riscul de cancer? Ce rol au micronutrienții, mitocondriile și microbiomul intestinal în răspunsul la tratamentul oncologic? Poate o alimentație personalizată să susțină vindecarea și să prevină recidivele?
Aceste aspecte au fost abordate în cadrul webinarului „Nutriția în cancer: de la regenerare mitocondrială la intervenție nutrițională în oncologie”, organizat de Zenyth Better Medicine. Lectorul webinarului, nutriționist-dietetician Camelia Râtea, specialist nutriție clinică și comunitară, competențe în Genomica Cancerului și Oncologie de Precizie (Harvard Medical School SUA), în Biologia cancerului (Universitatea Johns Hopkins SUA), membru al Societății Europene de Oncologie Medicală UE, membru al Asociației Americane de Nutriție, a prezentat modul în care nutriția influențează prevenția și managementul cancerului, subliniind importanța suportului nutrițional pe parcursul tratamentului oncologic. Micronutrienții, fitonutrienții și intervențiile nutriționale personalizate pot sprijini funcția mitocondrială, sistemul imunitar și regenerarea organismului, oferind strategii practice pentru optimizarea sănătății și prevenirea recidivelor.
Cuprins articol:
- Rolul nutriției în prevenția și managementul cancerului.
- Impactul micronutrienților asupra mitocondriilor și sistemului imunitar.
- De ce nutriția personalizată contează în fiecare etapă: de la diagnostic la remisie.
- Cum putem susține pacienții oncologici prin intervenții nutriționale țintite?
- Fitonutrienți (curcumină, resveratrol, EGCG, quercetină, acid elagic) și biogeneza mitocondrială.
- Antioxidanții și prevenția cancerului. Echilibrul redox: când antioxidanții ajută și când pot dăuna.
- N-acetilcisteina (NAC) și resveratrolul în contextul prevenirii și tratamentului cancerului.
- Rolul dietei în terapia adjuvantă oncologică (dieta ketogenică, fasting mimicking diet).
- Efectul nutriției asupra microbiomului și imunoterapiei.
- Intervenții dietetice pentru sarcopenie, cașexie, inflamație cronică.
Rolul nutriției în managementul cancerului
În ultimul deceniu, la nivel mondial, se observă o creștere semnificativă a cazurilor de cancer, în paralel cu îmbătrânirea populației și expunerea continuă la factori de stres oxidativ, poluare, sedentarism și diete dezechilibrate. Potrivit Globocan 2022, se estimează că până în 2040, incidența globală a cancerului va crește cu peste 50%, punând presiune majoră pe sistemele de sănătate deja suprasolicitate.
Un articol recent publicat în Cell Death Discovery subliniază rolul esențial al transcripției mitocondriale în dezvoltarea și progresia cancerului. Cancerul este, în principal, o boală a biologiei celulare, caracterizată prin dezechilibrul dintre proliferare, diferențiere și apoptoză. Doar 5-10% dintre cazuri au cauze genetice, restul fiind asociate unui stil de viață dezechilibrat: dietă, fumat, alcool, sedentarism, obezitate, infecții și poluanți.
Intervențiile nutriționale orientate metabolic devin tot mai recunoscute ca o componentă esențială în recuperarea post-oncologică. Susținerea energetică prin alimentație:
- reduce sarcopenia.
- ameliorează răspunsul imun.
- îmbunătățește toleranța la tratament.
- susține refacerea tisulară.
- poate reduce rata recidivelor tumorale.
Printre strategiile validate științific, se numără:
- aportul optim de proteine (1,5–2 g/kg corp).
- suplimentarea cu antioxidanți mitocondriali (Q10).
- corectarea deficitelor de vitamina D3, zinc și magneziu.
- alimentele fermentate natural și compușii bioactivi (ex: polifenoli, curcumină, omega-3).
Unde se produce energia în celulă?
În celulele eucariote, energia sub formă de ATP este produsă în principal în mitocondrii prin respirația celulară aerobă. Mitocondriile sunt considerate „uzinele energetice” ale celulei.
Teoria endosimbiotică explică originea acestora și vorbește despre înghițirea bacteriei aerobe, prin care celula ancestrală, probabil un eucariot primitiv sau archee, a încorporat o bacterie capabilă de respirație aerobă. Ulterior s-a produs trecerea de la relație facultativă la una obligatorie, iar relația simbiotică a devenit benefică pentru ambele părți, bacteriile producând ATP pentru gazdă, în timp ce celula gazdă oferă nutrienți și un mediu protejat. Următoarea etapă a fost transferul genelor, prin care multe gene ale bacteriei au fost transferate în nucleul celulei gazdă, ceea ce a făcut ca mitocondria să devină dependentă de celula gazdă pentru supraviețuire. În final, s-a produs integrarea completă, bacteriile și-au pierdut independența și au devenit organite specializate.
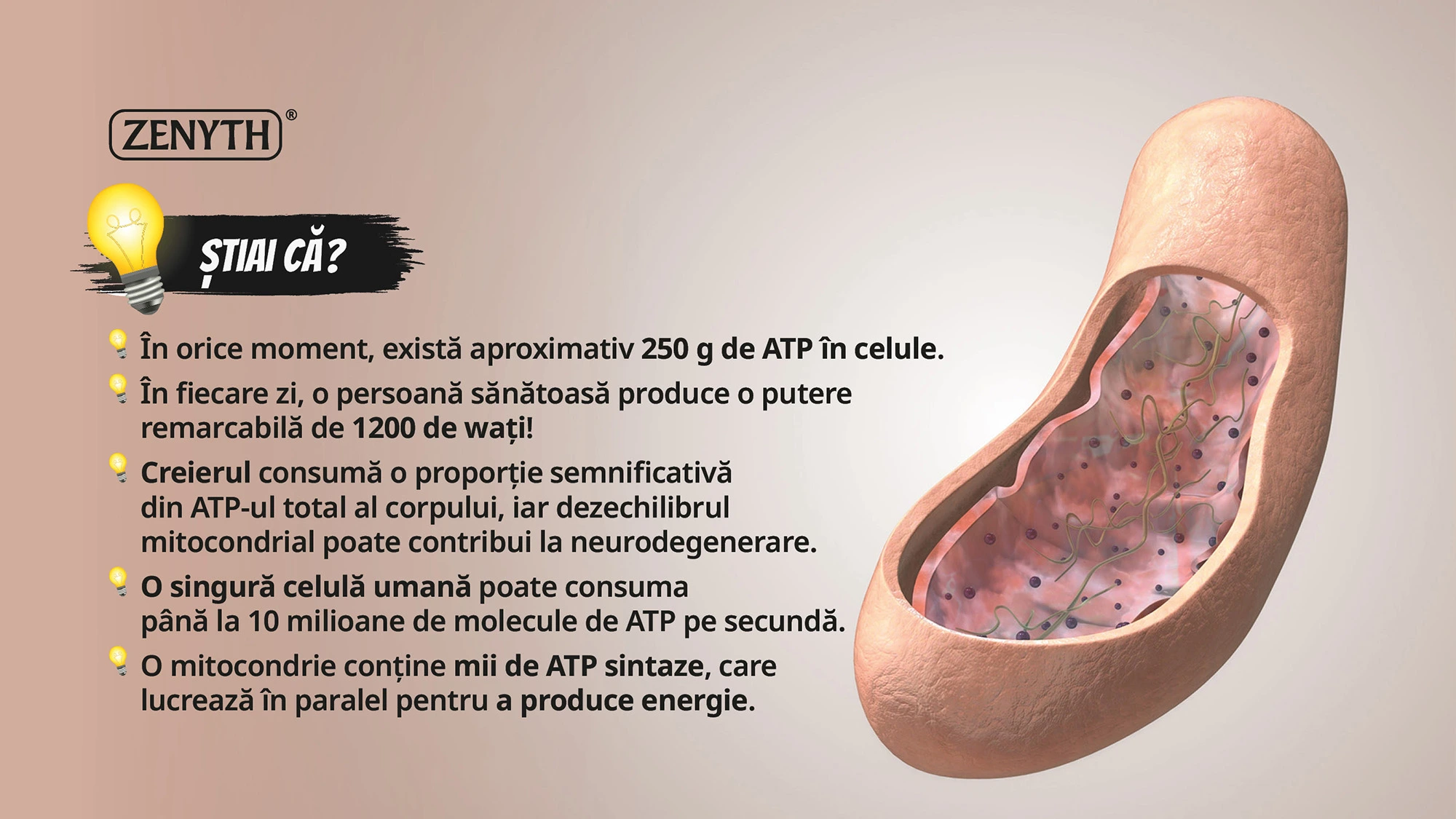
Mitocondria este o parte a celulei care funcționează ca o centrală energetică, generând cea mai mare parte a aprovizionării cu ATP (adenozin trifosfat), principala sursă de energie chimică pentru celulă. Mitocondriile sunt implicate în reglarea apoptozei și a metabolismului. Dieta bogată în antioxidanți naturali susține sistemele endogene de apărare celulară, prevenind daunele oxidative la nivelul ADN-ului și mitocondriilor.
Organismul nu poate stoca ATP, prin urmare mitocondriile trebuie să funcționeze constant tot timpul.
În cancer, mitocondriile au roluri complexe:
- Mutațiile în ADN-ul mitocondrial pot altera funcționarea lanțului de transport al electronilor, favorizând un metabolism anaerob (efectul Warburg) și susținând proliferarea celulară necontrolată.
- Procesul de mitofagie, prin care celulele elimină mitocondriile disfuncționale, este esențial pentru menținerea homeostaziei celulare. În cancer, dereglarea mitofagiei poate contribui la acumularea de mitocondrii defectuoase, promovând supraviețuirea celulelor tumorale.
- UPRmt (proteine nepliate) este un mecanism de protecție activat în condiții de stres mitocondrial. În celulele canceroase, activarea UPRmt poate susține adaptarea la condiții adverse și poate conferi rezistență la terapii.
Pe parcursul tratamentului oncologic, bolnavii dezvoltă frecvent disfuncții mitocondriale secundare, care pot duce la pierdere de masă musculară, fatigabilitate cronică, afectarea funcției cognitive, dezechilibre redox persistente și compromiterea sistemului imunitar. Aceste efecte contribuie la ceea ce literatura definește drept „colaps mitocondrial funcțional”, agravat de malnutriție, inflamație sistemică și epuizare energetică celulară. Acest concept, descris de Wallace (Nat Rev Cancer, 2012), subliniază rolul central al mitocondriei în fiziopatologia răspunsului la stres oncologic și susține necesitatea unor strategii de susținere metabolică și mitocondrială pe parcursul tratamentului.
Disfuncțiile mitocondriale și malnutriția proteică sunt fenomene frecvente în oncologie, influențând direct rata de răspuns la tratament, riscul de complicații și calitatea vieții bolnavului.
Strategiile de îmbunățire a disfuncției mitocondriale includ:
- Postul intermitent.
- Evitarea substanțelor toxice.
- Reducerea stresului: Stresul crește producția de cortizol, ducând la creșterea stresului oxidativ și afectarea funcției mitocondriale. Studiile recente arată că meditația de tip mindfulness, yoga, tehnicile de respirație controlată și expunerea la natură pot reduce nivelul de cortizol și pot îmbunătăți performanța energetică celulară.
- Somnul adecvat.
- Exercițiul fizic regulat: Exercițiul aerobic moderat poate îmbunătăți sănătatea mitocondrială prin stimularea biogenezei mitocondriale.
Procesul de producere a energiei este dependent de ATP sintază, o enzimă esențială localizată în membrana mitocondrială internă. ATP sintaza funcționează ca o turbină moleculară care utilizează protonii (H⁺) din gradientul electrochimic pentru a genera ATP (adenozin trifosfat).
Pentru funcționarea și sinteza ATP sintazei sunt necesari anumiți nutrienți. Printre aceștia, se numără aminoacizii esențiali, precum lizina, leucina, valina și izoleucina, care asigură construcția proteinelor mitocondriale.
Mitocondriile necesită o membrană lipidică sănătoasă pentru ancorarea ATP sintazei. Nutrienții necesari pentru menținerea acestei structure sunt:
- Acizi grași omega-3 și omega-6, care susțin integritatea membranei mitocondriale.
- Magneziul, ce stabilizează structura ATP.
- Cardiolipina, un fosfolipid specific mitocondriilor, esențial pentru stabilizarea ATP sintazei în membrana mitocondrială. Cardiolipina conține acizi grași polinesaturați, precum acidul linoleic. O dietă bogată în acești acizi poate susține structura și funcția cardiolipinei, prin consumul de ulei de șofrănel, semințe de in, nuci, migdale și pește gras.
- Electroliții, cum ar fi potasiul și sodiul, care ajută la menținerea gradientului electrochimic necesar pentru funcționarea ATP sintazei.
- Coenzima Q10.
Nutriția în prevenția cancerului
Nutriția influențează în mod direct riscul de cancer. Genomica nutrițională (nutrigenomica) oferă noi perspective asupra modului în care alimentele influențează expresia genelor și prevenția cancerului. Dietele pot influența metilarea ADN-ului și acetilarea histonelor, cu impact asupra expresiei genelor supresoare tumorale sau oncogene.
Zincul, seleniul, vitaminele A, C, E, flavonoidele și polifenolii sunt micronutrienți cu roluri cheie în apărarea antioxidantă, reglarea imunității și controlul epigenetic. Vitamina E are efecte anticancerigene prin acțiunea antioxidantă și prin reglarea expresiei genelor implicate în inflamație și apoptoză. Există studii care indică un posibil efect protector al vitaminei E în reducerea cancerului de prostată la bărbații cu risc crescut. Totuși, pe baza datelor disponibile, rolul său în prevenția cancerului rămâne încă amabiguu.
Quercetina, un flavonoid natural, are efecte protectoare, demonstrând în studii o asociere inversă cu riscul de cancer gastric, colorectal și pulmonar, mai ales la fumători. Carotenoizii, precum beta-carotenul, licopenul, luteina și zeaxantina, au efect antioxidant și potențial antitumoral. Un aport alimentar crescut este asociat cu risc scăzut de cancer, însă suplimentele cu beta-caroten pot crește riscul de cancer pulmonar la persoanele care deja au factori de risc, cum ar fi fumătorii. În concluzie, antioxidanții naturali pot contribui la prevenția cancerului, dar efectele depind de contextul individual.
Impactul micronutrienților asupra mitocondriilor și sistemului imunitar
Micronutrienții precum coenzima Q10, magneziul, zincul, seleniul și manganul sunt esențiali pentru funcționarea optimă a mitocondriilor, influențând metabolismul celular și apoptoza. Aceștia susțin răspunsul imun, contribuind la detectarea și eliminarea celulelor tumorale.
Coenzima Q10 este cofactor în lanțul de transport al electronilor, susține producția de ATP și reduce stresul oxidativ mitocondrial. Ca efect asupra sistemului imunitar, reduce citokinele proinflamatorii și este un modulator al inflamației. Există studii pe pacienți cu insuficiență cardiacă, boli cronice și unele studii pilot în cancer.
Magneziul este cofactor în peste 300 de reații enzimatice și este implicat în stabilitatea ADN-ului mitocondrial și fosforilarea oxidativă. Acesta este esențial pentru funcția limfocitelor T și B. Deficitul de magneziu este asociat cu inflamația cronică. Despre acțiunile sale sunt diponibile dovezi robute din studii nutriționale.
Zincul protejează mitocondriile împotiva stresului oxidativ și reglează biogeneza mitocondrială. În plus, susține imunitaea înnăscută și adaptativă, are efect antiviral și rol în producția de interleukine. Studii clinice și intervenționale în infecții, imunitate și cancer.
Seleniul este cofactor pentru enzime antioxidante mitocondriale (ex: glutation peroxidază). Este imunomodulator: reglează răspunsul Th1/Th2 și susține funcția natural killer. Există dovezi solide privind rolul său în anumite tipuri de cancer, precum cel de prostată și cel tiroidian, iar deficitul de seleniu este frecvent asociat cu scăderea funcției imunitare.
Manganul este cofactor pentru MnSOD, o enzimă crucială în detoxifierea radicalilor liberi în mitocondrii. Are un efect indirect asupra sistemului imunitar, prin protecția mitocondrială reduce inflamația sistemică. Majoritatea dovezilor sunt preclinice sau observaționale. Suplimentarea cu mangan trebuie atent aleasă în funcție de etapa în care se află pacientul oncologic. Poate fi folosită mai degrabă ca prevenție, iar în stadiile incipiente de regulă previne acumularea de radicali liberi, dar cu atenție în tratamentele prelungite.
De ce nutriția personalizată contează în fiecare etapă: de la diagnostic la remisie
Nutriția personalizată ține cont de profilul genetic, metabolic și imunologic al fiecărui pacient. Adaptarea alimentației în funcție de tipul și stadiul cancerului poate îmbunătăți răspunsul la tratament și calitatea vieții.
Testele de nutrigenetică, markerii inflamatori, analiza microbiomului și evaluarea statusului antioxidant permit ajustarea precisă a intervențiilor nutriționale la nevoile individuale. O astfel de abordare sprijină organismul încă din momentul diagnosticului, reduce efectele adverse ale terapiilor și favorizează recuperarea post-tratament, contribuind la scăderea riscului de recidivă.
În etapa de remisie, nutriția individualizată devine o componentă esențială a recuperării oncologice, cu potențialul de a restabili echilibrul metabolic, de a reduce stresul mitocondrial și de a optimiza markerii inflamatori și nutriționali.
Cum putem susține pacienții oncologici prin intervenții nutriționale țintite?
Suportul nutrițional în oncologie include corectarea deficitelor de micronutrienți, asigurarea unui aport proteic adecvat, suplimentarea cu nutrienți mitocondriali și integrarea fitonutrienților cu rol antiinflamator și antioxidant. Astfel de intervenții reduc inflamația, sprijină regenerarea țesuturilor, protejează celulele sănătoase și îmbunătățesc toleranța la tratamente.
Fitonutrienți și biogeneza mitocondrială

Biogeneza mitocondrială este procesul prin care celula crește numărul și funcționalitatea mitocondriilor. Are un rol important pentru homeostazia energetică, adaptarea la stres și repararea mitocondrială.
Există o serie de compuși bioactivi precum curcumina, resveratrolul, EGCG din ceaiul verde, quercetina și acidul elagic, care stimulează biogeneza mitocondrială. De asemenea, Urolitin A este un metabolit al polifenolilor intestinali, care stimulează mitofagia și biogeneza.
Dovezile experimentale și studiile pe animale arată că suplimentarea cu resveratrol și urolitin A susține îmbunătățirea funcției mitocondriale. Studiile clinice timpurii au observat că resveratrolul și quercetina arată îmbunătățiri în boli metabolice (ex: diabet, obezitate), legate de activarea mitocondrială.
Proteazomul este un complex din celulă care degradează proteinele inutile, deteriorate sau modificate, menținând celula sănătoasă. Celulele canceroase sunt mai sensibile la inhibitorii de proteazom decât cele normale, ceea ce face din această cale o țintă importantă în terapia oncologică și chemoprevenție. Inhibarea proteazomului poate opri ciclul celular și induce apoptoza, mecanism exploatat în tratamente precum cele pentru mielom multiplu sau limfoame.
Mai mulți compuși naturali au efect de inhibare a proteazomului. EGCG din ceai verde, genisteina din soia, curcumina din turmeric, flavonoidele (apigenina, quercetina, luteolina), withaferin A din ginseng indian și celastrolul din Tripterygium wilfordii au demonstrat că pot bloca activitatea proteazomului în celulele tumorale și pot induce apoptoza, fără a afecta celulele normale.
Antioxidanții și prevenția cancerului. Echilibrul redox: când antioxidanții ajută și când pot dăuna
Antioxidanții au un rol dual, putând proteja celulele sănătoase de stresul oxidativ, dar în anumite condiții pot interfera cu tratamentele oncologice. Menținerea unui echilibru redox adecvat este crucială pentru prevenirea și tratamentul eficient al cancerului.
În timpul chimioterapiei și radioterapiei, unul dintre mecanismele principale este generarea de ROS (specii reactive de oxigen) pentru a se induce moartea celulelor tumorale. Ca interferențe posibile, antioxidanții pot reduce eficiența tratamentului, neutralizând ROS necesari pentru distrugerea celulelor canceroase. Studiile in vitro și in vivo au arătat că suplimentarea cu antioxidanți în timpul tratamentului poate reduce stresul oxidativ indus de citostatice, limita apoptoza indusă de ROS în celulele tumorale și favoriza supraviețuirea celulelor canceroase rezistente.
N-acetil cisteina (NAC) și resveratrolul în contextul prevenirii și tratamentului cancerului
N-acetil cisteina (NAC) este un antioxidant și precursor de glutation, care protejează celulele sănătoase de stresul oxidativ. S-a observat că aceasta poate inhiba proliferarea anumitor celule canceroase, inclusiv de prostată, de colon și de sân. NAC inhibă proliferarea celulelor de cancer de prostată PC-3 (androgen independent) prin mecanisme ce implică stres oxidativ și semnalizare celulară, într-un mod dependent de doză și timp. La 2 ore după administrare are efect antioxidant (reduce ROS), iar la 48 ore, efect pro-oxidant, crescând nivelul ROS.
N-acetil cisteina poate reduce efectele adverse ale chimioterapiei (ex: toxicitate pulmonară, hepatotoxicitate, nefrotoxicitate). Poate interfera cu tratamentele care depind de stres oxidativ pentru a ucide celulele canceroase, cum ar fi chimioterapia, radioterapia, terapia cu inhibitori ai proteazomilor.
Resveratrolul, polifenol natural cu proprietăți antioxidante, acționează ca un fitoestrogen, având capacitatea de a se lega de anumiți receptori estrogenici. Această activitate duală îl face un compus cu efecte controversate în cancer: pe de o parte, unele studii indică efecte anticancerigene (prin modularea inflamației, a angiogenezei și a proliferării celulare), iar pe de altă parte, în cancerele sensibile la hormoni (de exemplu, cancerul de sân ER+ sau unele forme de cancer de prostată), resveratrolul poate stimula proliferarea și dezvoltarea tumorilor. Astfel, efectele sale depind de contextul biologic, de tipul de cancer și de doză.
În ansamblu, antioxidanții precum NAC și resveratrolul pot avea un rol protector în prevenția cancerului, protejând celulele sănătoase de daune oxidative. Însă, în timpul tratamentelor oncologice, aceștia pot deveni o armă cu două tăișuri, având potențialul de a reduce eficiența terapiilor care se bazează pe stres oxidativ pentru a ucide celulele tumorale.
Rolul dietei în terapia adjuvantă oncologică
Dietele metabolice, precum cea ketogenică sau dieta care mimează postul (Fasting Mimicking Diet – FMD), influențează metabolismul tumoral și pot spori eficiența terapiilor oncologice. Acestea reduc inflamația, protejează celulele sănătoase și pot scădea toxicitatea chimioterapiei și radioterapiei.
Studiul DIRECT (Dietary Restriction with Chemotherapy) a analizat efectele dietei care mimează postul (fasting mimicking diet) asupra eficacității și tolerabilității chimioterapiei la paciente cu cancer de sân HER2-negativ. Rezultatele sugerează că FMD poate crește eficiența tratamentului, reduce efectele adverse și îmbunătăți răspunsul tumoral, mai ales atunci când regimul este urmat cu strictețe. Totuși, acest tip de dietă nu este recomandat tuturor pacientelor, în special celor cu risc de malnutriție sau cașexie. De aceea, inițierea unei astfel de intervenții nutriționale trebuie făcută doar sub supravegherea medicului oncolog și a unui nutriționist specializat.
Dieta ketogenică este bogată în grăsimi, săracă în carbohidrați, imitând starea metabolică de foame și inducând cetoză. Aceasta reduce nivelul glicemiei și insulinei și forțează organismul să utilizeze corpi cetonici (ex: beta-hidroxibutirat) în loc de glucoză pentru energie. Celulele canceroase (inclusiv cele din glioblastom) preferă glucoza, iar dieta ketogenică poate „înseta” tumora de combustibil energetic.
În schimb, diete precum cea alcalină, Gerson sau regimurile vegane/raw nu au dovezi clinice solide și pot duce la deficiențe nutriționale. Totodată, dieta neutropenică (evitarea alimentelor crude/nepasteurizate) nu și-a confirmat eficiența în reducerea infecțiilor. Se recomandă mai degrabă manipularea sigură a alimentelor, nu excluderea alimentelor proaspete. Alimentația echilibrată, bogată în fibre, legume, acizi grași omega-3, soia și lactate cu conținut redus de grăsimi, susținută de dovezi epidemiologice și ghiduri clinice (WCRF/AICR), rămâne una dintre cele mai solide recomandări pentru sprijinirea supraviețuirii și reducerea recidivelor oncologice.
Studiile arată că curcumina și alte molecule din plante (polifenolii din ceai verde, silibina din armurariu, kaempferolul din broccoli, luteolina din țelină, ardei verde) pot avea rol adjuvant în terapia oncologică, prin reducerea inflamației, inhibarea semnalizării STAT și inducerea apoptozei celulelor tumorale. Efectele depind însă de tipul cancerului și de chimioterapia administrată, unele combinații putând reduce eficacitatea tratamentului. Formulele cu biodisponibilitate crescută (Longvida®, Meriva®) sunt preferabile, iar suplimentele trebuie administrate cu atenție, sub supraveghere medicală.
Efectul nutriției asupra microbiomului și imunoterapiei
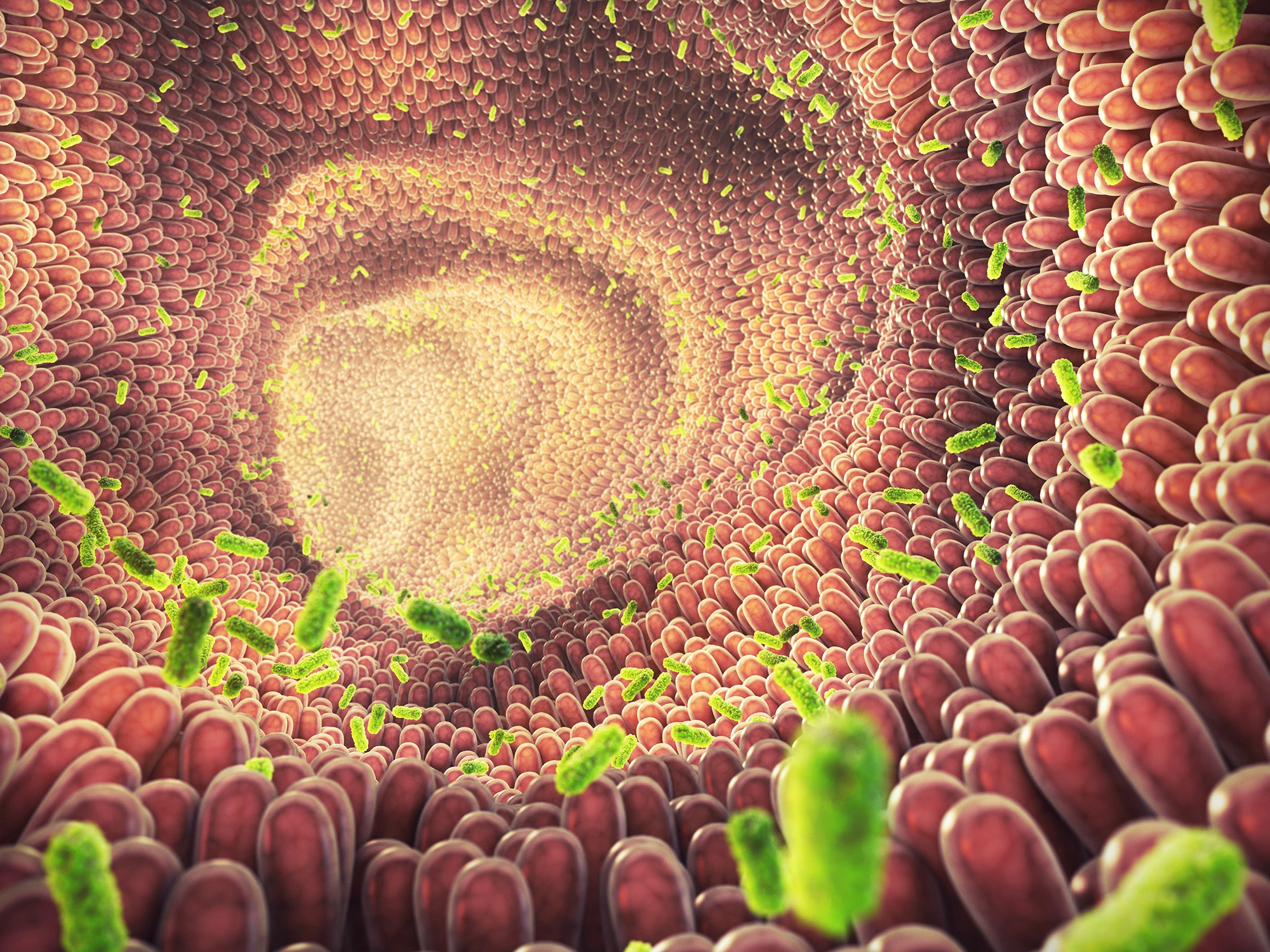
Compoziția microbiotei este influențată de dietă și afectează răspunsul imun, inflamația și metabolizarea compușilor cancerigeni sau protectivi. Microbiomul intestinal are un rol esențial în modularea răspunsului la imunoterapie. O dietă bogată în fibre, alimente fermentate și polifenoli susține diversitatea microbiană și sporește eficiența tratamentelor oncologice. Dezechilibrele microbiotei, pe de altă parte, pot reduce eficacitatea imunoterapiei și pot favoriza inflamația cronică.
În zona de nutriție, este importantă menținerea integrității joncțiunilor intestinale, care influențează modul în care celulele imune accesează și recunosc celulele tumorale. Disfuncția acestor joncțiuni poate duce la permeabilitate intestinală (permite translocarea bacteriană, creând un mediu pro-tumoral), modificări în expresia occludinei și claudinelor (pot reduce eficacitatea imunoterapiei) și niveluri crescute de zonulină (asociate cu prognostic slab în anumite tipuri de cancer, sugerând un rol în rezistența la tratamente). Occludinele, claudinele și zonulina sunt proteine esențiale în menținerea integrității joncțiunilor strânse (tight junctions) ale epiteliilor.
S-a observat că prebioticul PHGG (guma guar parțial hidrolizată) contribuie la întărirea joncțiunilor strânse ale epiteliului intestinal și la reducerea permeabilității intestinale. Deși este, în general, bine tolerat, PHGG ar trebui evitat sau monitorizat cu atenție la persoanele cu ocluzie intestinală, neutropenie severă sau cu tulburări digestive active severe.
Intervenții dietetice pentru sarcopenie, cașexie, inflamație cronică
Sarcopenia și cașexia sunt probleme frecvente în oncologie, asociate cu un prognostic rezervat. Sarcopenia este caracterizată prin scăderea progresivă de masă musculară, care poate duce la afectare funcțională și scăderea calității vieții.
Cașexia este o pierdere severă și involuntară de greutate, în special de masă musculară (și uneori și de grăsime), ce apare în contextul unor boli cronice. Dereglarea funcției mitocondriale contribuie la degradarea musculară și la pierderea masei corporale. Pe lângă semnele clinice precum pierdere în greutate semnificativă în ultimele 6 luni și IMC mai mic de 20, semnele metabolice sunt inflamația (CRP crescut), anorexia, oboseala, scăderea forței musculare. Cașexia afectează până la 80% dintre pacienții cu cancer în stadii avansate. Aceasta scade toleranța la tratamente (chimioterapie, radioterapie), crește toxicitatea și riscul de deces.
Intervenția dietetică este esențială în toate etapele îngrijirii oncologice, mai ales la apariția riscului de malnutriție sau la pierderi semnificative de greutate. Intervențiile nutriționale recomandate includ un aport proteic ridicat (1,5–2 g/kg corp), suplimentarea cu omega 3 (în special EPA 1,4 -2 g/zi) și consumul de fitonutrienți antiinflamatori. Se recomandă mese mici și frecvente, alimente dense caloric și proteic (ouă, avocado, supe concentrate, unt), adaptate simptomelor digestive.
Pentru disfagie sau inflamații bucale, se recomandă alimente pasate sau lichide îngroșate. În caz de alterare a gustului, pot fi utile alimentele reci sau la temperature camerei, texturile moi și evitarea tacâmurilor metalice. Aceste măsuri sprijină evitarea declinului nutrițional, imunitatea și îmbunătățirea calității vieții în timpul tratamentelor oncologice.
În încheiere, lectorul webinarului, nutriționist-dietetician Camelia Râtea, a subliniat că testarea markerilor funcționali mitocondriali (lactat/piruvat), inflamatori și nutriționali (prealbumină) permite intervenții nutriționale țintite în recuperarea oncologică. Alimentația nu doar că joacă un rol esențial în prevenția cancerului, ci și susține tratamentele oncologice prin influențarea căilor moleculare și stimularea regenerării mitocondriale.
Webinarul „Nutriția în cancer: de la regenerare mitocondrială la intervenție nutrițională în oncologie” face parte din seria de webinare Zenyth – Better Medicine. Pentru a participa la următoarele webinare, te invităm să te înscrii la newsletter-ul nostru și vei primi invitații la evenimentele Better Medicine.
Resurse:
- Hood S, Amir S. The aging clock: circadian rhythms and later life. J Clin Invest. 2017.
- Stenvers DJ et al. Circadian clocks and insulin resistance. Nat Rev Endocrinol. 2019.
- Wacquier B et al. The Impact of Sleep on Mitochondrial Function. Front Cell Dev Biol. 2022.
- Prado et al., Lancet Oncology, 2008 – „Sarcopenia predicts toxicity and survival in cancer.”
- Fearon et al., Nature Reviews Clinical Oncology, 2012 – „Definition and classification of cancer cachexia”
- S. DiMauro, E. A. Schon. Mitochondrial respiratory-chain diseases. New England Journal of Medicine, 2003.
- Alberts et al., Molecular Biology of the Cell, 6th Edition
- Fasting-mimicking diet plus chemotherapy in breast cancer treatment,Claudio Vernieri, Francesca Ligorio, Emma Zattarin, Licia Rivoltini & Filippo de Braud ,Nature Communications volume 11, Article number: 4274 (2020)
- Resveratrol fuels HER2 and ERα-positive breast cancer behaving as proteasome inhibitor-Cristina Andreani,Caterina Bartolacci ,Kathleen Wijnant, Rita Crinelli,Marzia Bianchi,Aging (Albany NY). 2017 Feb 26;9(2):508–520
- Zhang Y, Wang Y, Li Y, et al. Resveratrol supplementation reduces inflammatory markers: A systematic review and meta-analysis of randomized controlled trials. Clin Ther. 2018;40(7):1180-1192.e5. oi:10.1016/j.clinthera.2018.05.015
- Wang L, Li J, Zhang Y, et al. Resveratrol promotes the proliferation of HER2 and ERα-positive breast cancer cells by activating estrogen receptor signaling. Carcinogenesis. 2017;38(8):781-790. doi:10.1093/carcin/bgx059
- „Effects of a ketogenic diet on the quality of life in 16 patients with advanced cancer” – Nutrition & Metabolism













