Cuprins
Bariera hematoencefalică și microglia în patogeneza anxietății și depresiei
Factori genetici în PANS
Ganglionii bazali
Vulnerabilitatea lenticulostriată
Sistemul limbic. PANS ca tulburare de stres posttraumatic
Manifestările obsesiv-compulsive
Agresivitatea
PANS/PANDAS și tulburarea de spectru autist
Declanșatori
Caracterizare metabolomică
PANS și disbioza intestinală
Concluzii
Bibliografie
Bariera hematoencefalică și microglia în patogeneza anxietății și depresiei
Bariera hematoencefalică are o suprafață totală de aproximativ 20 m2 și constituie o delimitare fizică, metabolică și imunologică a creierului față de sistemul circulator.
Creșterea permeabilității barierei se realizează prin mecanisme fiziopatologice complexe ca stresul oxidativ, neuroinflamația și degradarea joncțiunilor.
Afectarea acestei bariere expune mediul fragil al creierului la substanțe potențial periculoase, ducând la pierderea homeostaziei prin dezechilibre ionice și nutriționale și la afectarea semnalizării neuronale. O afectare mai gravă determină extravazarea proteinelor serice și edem cerebral.
Sistemul nervos central răspunde la inflamația sistemică prin activarea microgliei, sinteza de citokine proinflamatorii și factori de creștere și prin transmiterea exagerată a durerii (hiperalgezie).
Mediatorii inflamatori produși de creier afectează din interior bariera hematoencefalică, iar mediatorii inflamatori sistemici o afectează din exterior.
IL-17A și IFN-γ afectează joncțiunile endoteliale in vitro și in vivo. Bariera hematoencefalică devine permeabilă la proteine serice nu numai când aceste joncțiuni sunt distruse, ci și când transcitoza este intensificată în celulele endoteliale. [40]
Un studiu din 2025 arată că nivelul de oxLDL, indicator de stres oxidativ și inflamație, se corelează invers cu nivelul de Zonula occludens protein – 1 (ZO-1) și occludin, indicatori ai integrității barierei hematoencefalice. Pacienții cu depresie majoră au niveluri scăzute de ZO-1 și occludin și niveluri crescute de oxLDL.
Experimente realizate pe șoareci au arătat că microglia răspunde la inflamația sistemică generată de LPS în două etape. La început, microglia migrează spre bariera hematoencefalică pentru a-i proteja integritatea. Dacă inflamația continuă, se intră în etapa a doua, când microglia se transformă într-un fenotip reactiv care fagocitează componentele barierei hematoencefalice. Se realizează astfel o creștere a permeabilității, ceea ce permite mediatorilor inflamatori să intre în creier și să agraveze inflamația.
Stresul psihosocial duce la eliberarea în circulație a monocitelor proinflamatorii, producătoare de IL-1β. Acestea activează microglia care generează anxietate prin mecanism inflamator. [38]
Infecția cu Staphylococcus aureus și sărurile de aluminiu induc eliberarea de IL-1β prin activarea inflamazomului NLRP3. Infecția cu Salmonella typhimurium, Shigella flexneri, Legionella pneumophila, and Pseudomonas aeruginosa induce eliberarea d IL-1β prin activarea inflamazomului NLRC4. Se cunoaște faptul că aceste infecții sunt corelate cu anxietatea, depresia și alte tulburări neuropsihice.
Factori genetici în PANS
Un studiu publicat în 2022 a descoperit în unele cazuri grave de PANS modificări genetice în două categorii de gene: prima categorie reglează răspunsul imun periferic și microglia (PPM1D, CHK2, NLRC4, RAG1, PLCG2), iar a doua este exprimată în principal în sinapse (SHANK3, SYNGAP1, GRIN2A, GABRG2, CACNA1B, SGCE). Mutații în aceste gene au fost constatate și în unele cazuri de TSA. [50]
Ganglionii bazali
Componentele centrale ale ganglionilor bazali sunt situate în telencefal și includ globus pallidus și striatum (ansamblu format din nucleul caudat și putamen – dorsal și nucleus accumbens – ventral).
Nucleii asociați ai ganglionilor bazali sunt situați în diencefal (nucleul subtalamic) și mezencefal (substantia nigra și nucleul pedunculopontin).
Din punct de vedere funcțional, nucleii ganglionilor bazali sunt de intrare (input), de ieșire (output) și intermediari.
Nucleii de intrare cuprind striatum, nucleus accumbens și tuberculul olfactiv. Ei primesc aferențe de la cortex și talamus.
Nucleii de ieșire cuprind globus pallidus partea internă și substantia nigra pars reticulata.
Aceștia realizează un control al talamusului care, la rândul lui, trimite semnale la cortex,
închizând bucla cortex-ganglioni bazali-talamus-cortex.
Nucleii intermediari cuprind globus pallidus partea externă, nucleul subtalamic și substantia nigra pars compacta.
Striatum conține două tipuri diferite de neuroni: neuroni de proiecție și interneuroni. Neuronii de proiecție cuprind aproximativ 90% din neuronii striatali și sunt neuroni inhibitori GABA ergici care primesc semnale corticale excitatoare.
Ei primesc, de asemenea, input dopaminergic modulator de la substantia nigra prin intermediul sistemul nigrostriatal. Acest input dopaminergic exercită efecte diferite, în funcție de tipul receptorilor dopaminergici.
Neuronii care se proiectează direct către globus pallidus interior conțin receptori de dopamină subtip 1 (receptori D1), care activează semnalizarea adenilil ciclazei și dau naștere căii directe (striatum – globus pallidus intern – talamus).
Când agoniștii se atașează de receptorii D1, este activată adenilil ciclaza, fapt care declanșează o cale de semnalizare ce conduce la deschiderea canalelor de calciu de tip L și închiderea canalelor de potasiu. Aceasta face ca neuronul să fie mai sussceptibil la depolarizare.
Stimularea receptorilor D1 produce o cascadă de fosforilare care crește activitatea receptorilor AMPA și NMDA, care intensifică răspunsul excitator.
Ganglionii striatali care ajung la globus pallidus extern exprimă receptorul de dopamină de subtip 2 (receptori D2), care inhibă adenililciclaza intracelulară și dau naștere la calea indirectă (striatum – globus pallidus extern – nucleul subtalamic – globus pallidus intern – talamus).
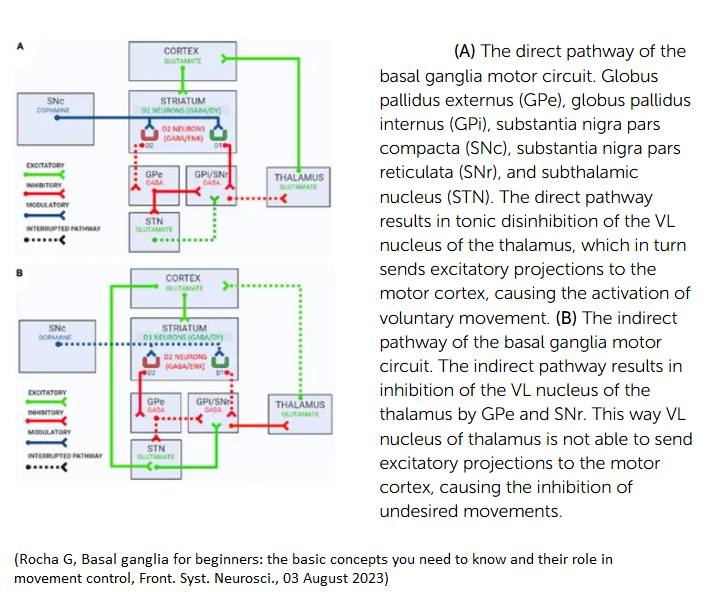
Inițial s-a crezut că cele două căi funcționează alternativ și antagonist. Însă acum cunoaștem că acestea lucrează sinergic și complementar.
Când începe mișcarea voluntară, ambele căi sunt activate. Neuronii căii directe selectează programul motor dorit, în timp ce calea indirectă inhibă celelalte programe motorii.
În afară de calea directă și cea indirectă, mai există și calea hiperdirectă, o conexiune axonală monosinaptică de la cortexul frontal la nucleul subtalamic. Aceasta utilizează glutamatul ca neurotransmițător și are rolul de a realiza o inhibiție rapidă pentru suprimarea acțiunii motorii.
Nucleul caudat și putamen intervin în inițierea mișcărilor, selectare și inhibiție prin calea directă și indirectă.
Nucleus accumbens integrează semnalele corticale și limbice pentru motivație, învățare, recompensă și luarea deciziilor.
Nucleul subtalamic este implicat în selectarea acțiunilor. Lezarea sau stimularea acestuia poate provoca disfuncții cognitive, tulburări de dispoziție, anxietate, iritabilitate, agresivitate, tulburări de alimentație, schimbări de personalitate.
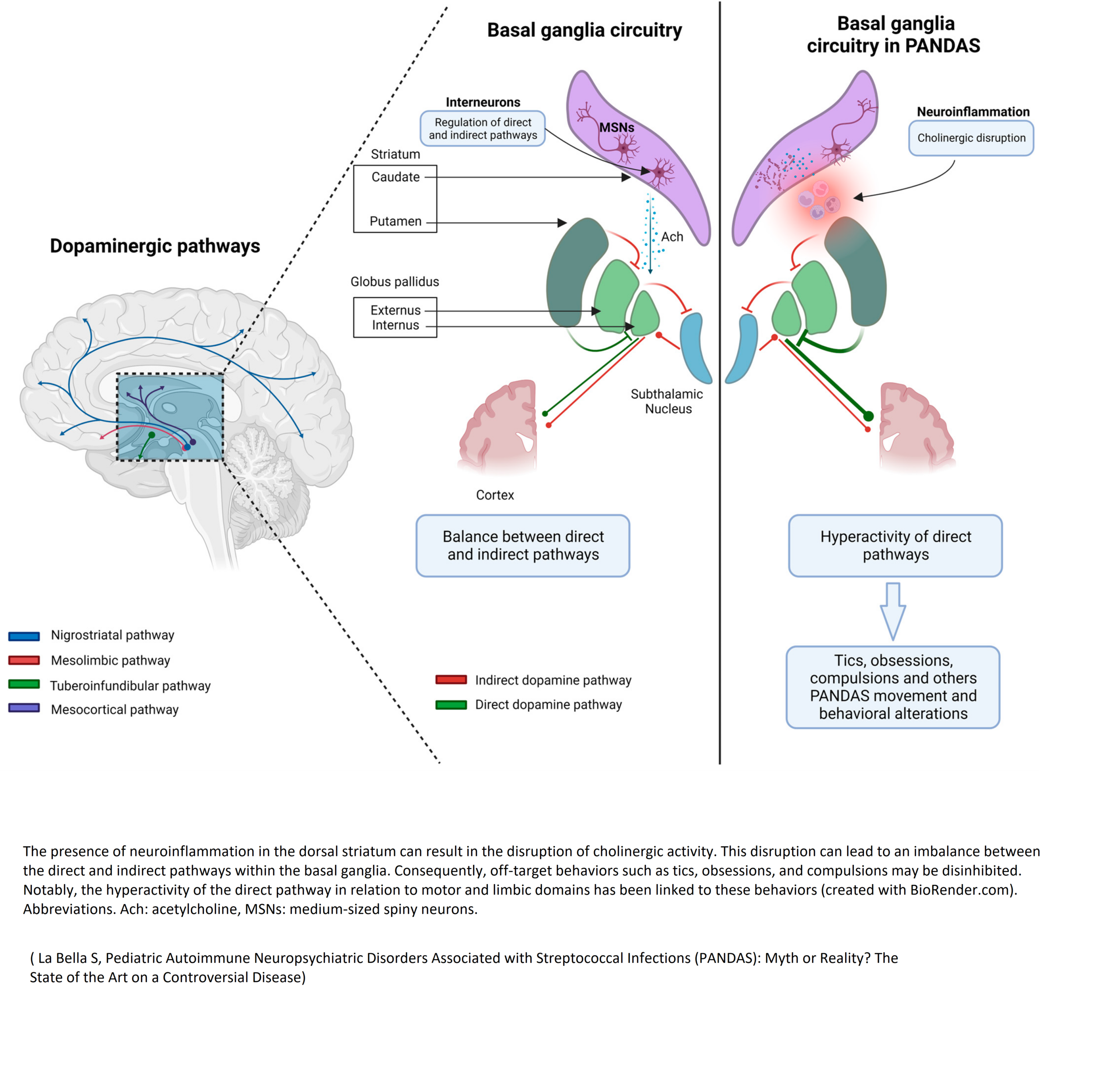
Vulnerabilitatea lenticulostriată
Aprovizionarea cu sânge a ganglionilor bazali este asigurată în principal de arterele lenticulostriate, ramuri ale arterei cerebrale mijlocii. Ele sunt unele dintre cele mai delicate structuri vasculare cerebrale.
Aceste artere prezintă o mare variabilitate, atât ca număr (între 1 și 14), cât și ca geometrie (arborescență). [3]
Au o vulnerabilitate mai mare și reprezintă o localizare importantă a hemoragiei la pacienți cu hipertensiune. Vulnerabilitatea lor se manifestă și în cazul atacului imunologic asupra barierei hematoencefalice.
Sistemul limbic. PANS ca tulburare de stres posttraumatic
Sistemul limbic este un complex de structuri cerebrale implicate în funcțiile autonome, generarea și reglarea răspunsurilor emoționale, memoria emoțională, învățare, motivație, comportament social, procesarea informațiilor olfactive.
Componentele principale sunt: hipocampul, amigdala, hipotalamusul, girusul cingular, corpii mamilari și nucleii septali.
Amigdala procesează emoțiile (în special frica) și le leagă de amintiri. Hipocampul intervine în procesarea amintirilor și orientarea spațială. Girusul cingular intervine în luarea deciziilor motivate emoțional. Nucleii septali intervin în motivație și în mecanismele recompensei.
Hiperactivarea amigdalei și dereglarea conexiunii cu cortexul prefrontal generează anxietate și fobii. De asemenea, tulburarea de stres posttraumatic (PTSD) este asociată cu hiperactivitatea amigdaliană și disfuncția hipocampului. Cazurile de PANS/PANDAS, în care copiii sunt hipervigilenți, îngroziți și agresivi, au trăsături comune cu tulburarea de stres posttraumatic. E important să înțelegem trăirile acestor copii și să aplicăm măsurile psihoterapeutice adecvate. De exemplu, în multe cazuri de PANS s-au dovedit utile cele trei măsuri luate pe timp de noapte: luminița de noapte (pentru siguranță), păturica (pentru protecție) și jucăria de pluș (pentru afectivitate). Părinții trebuie ajutați să înțeleagă faptul că acești copii trăiesc o puternică traumă psihică generată de neuroinflamație, fără eveniment psihotraumatizant exterior. Ei nu sunt obraznici sau îndărătnici, ci sunt efectiv îngroziți și reacționează firesc pentru o astfel de situație. Dr. Gabor Maté exprimă în mod optim această idee, spunând că tulburarea de stres posttraumatic nu este propriu zis o tulburare, ci o reacție firească la o situație nefirească.
Manifestările obsesiv-compulsive
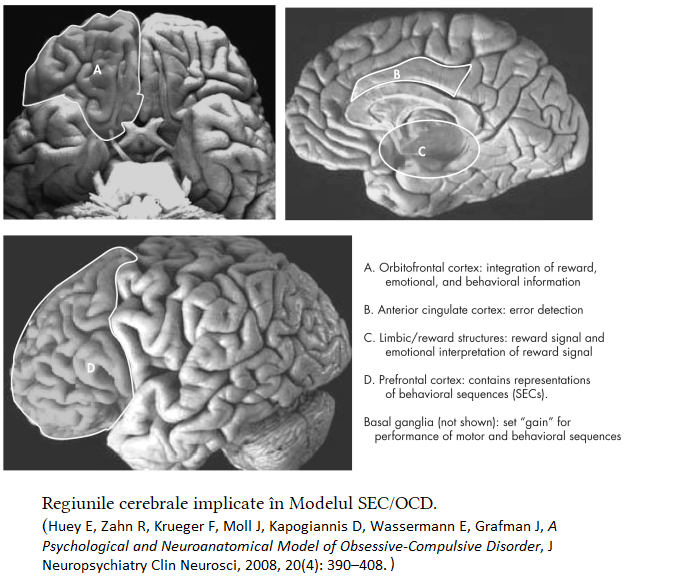
Studiile imagistice, chirurgicale și lezionale arată că în manifestările obsesiv-compulsive
sunt implicate următoarele structuri:
– cortexul orbitofrontal, în mecanismele recompensei;
– cortexul cingulat anterior, în detecția erorilor;
– cortexul prefrontal, în memorarea secvențelor comportamentale (SECs = Structured Event Complexes)
– ganglionii bazali, în stabilirea pragului de activare a programelor motorii și comportamentale;
În anul 2008 a fost propus modelul SEC/OCD (SEC=Structured Event Complex, OCD = Obsessive-Compulsive Disorder). Conform acestui model, o persoană sănătoasă, dacă are mâinile murdare, simte o anxietate motivațională pentru a efectua secvența de spălare a mâinilor. La finalizarea acestei secvențe, persoana primește ca recompensă o stingere a anxietății motivaționale. Persoanele cu manifestări obsesiv-compulsive nu primesc o stingere completă a acestei anxietăți la finalizarea secvenței, ci o ușoară atenuare. Acestea interpretează persistența anxietății motivaționale ca însemnând că mâinile lor sunt încă murdare, în ciuda faptului că le-au spălat. Deci secvența de spălare trebuie continuată. [25]
Acesta este un model de “încredere cumulativă”. Persoana nu dobândește încrederea că spălarea a fost eficientă și suficientă la finalizarea secvenței de spălare, ci încrederea se dobândește treptat, cumulativ, în urma repetării secvenței de spălare de un anumit număr de ori. Cu cât este mai mic “câștigul de încredere” la fiecare repetiție, cu atât mai multe secvențe de spălare sunt necesare.
Modelul se aplică și la obsesiile de verificare, de exemplu verificarea închiderii ușii sau a închiderii focului la aragaz. Deși persoana este conștientă că a închis ușa sau focul la aragaz, simte că nu a verificat suficient.

Pacienții cu manifestări obsesiv-compulsive au niveluri mai mari de IL-1β, IL-6 și TNF-α față de persoanele sănătoase, indicând implicarea neuroinflamației. [33]
Copiii și adolescenții cu PANS/PANDAS pot prezenta diverse manifestări obsesiv-compulsive:
Spălarea exagerată a mâinilor sau a corpului;
Obsesia alimentelor contaminate și cerința de a fi prelucrate termic pentru sterilizare;
Ordonarea exagerată a obiectelor, etc.
Agresivitatea
Amigdala furnizează informații importante cortexului orbitofrontal. Pe această cale se realizează modularea intensității agresivității și a expresiei acesteia, atât la agresivitatea direcționată spre exterior (vătămarea altora) cât și la cea direcționată spre propria persoană (auto-vătămare).
O conectivitate mai puternică între amigdală și cortexul orbitofrontal se corelează cu o mai bună reglare a furiei și o agresivitate redusă, în timp ce perturbările de conectivitate duc la o reactivitate sporită.
Disbioza intestinală influențează conectivitatea amigdalei și, prin aceasta, afectează reglarea furiei și permite o mai puternică exprimare a agresivității.
PANS/PANDAS și tulburarea de spectru autist
Mulți copii cu PANS/PANDAS au disbioză intestinală, iar unii au nivel mare de zonulin. De asemenea, mulți pacienți cu tulburare de spectru autist (TSA) au simptome gastrointestinale, iar la unii a fost pus în evidență un tipar de disbioză intestinală.
Un studiu publicat în 2017 arată că nivelul plasmatic de zonulin la un eșantion de pacienți cu TSA (122.3 ± 98.46 ng/mL) a fost semnificativ mai mare (P < .001) comparat cu lotul de control (41.89 ± 45.83 ng/mL). De asemenea, a existat o corelație pozitivă între nivelul de zonulin și scorul la Childhood Autism Rating Scale (r = 0.523; P < .001). [14]
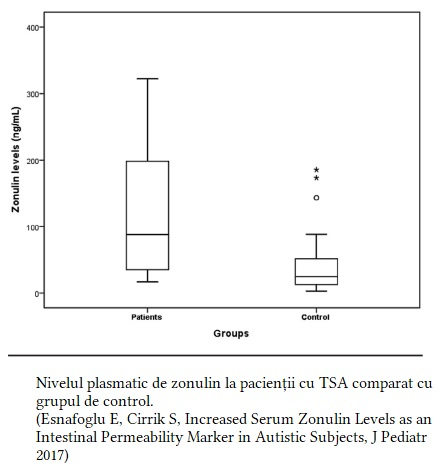
Putem considera starea generală a pacienților cu TSA ca fiind un teren predispozant pentru PANS/PANDAS. Atunci când o persoană cu TSA dezvoltă PANS, multe simptome de PANS se suprapun peste cele de TSA, fiind astfel mai greu se sesizat.
Declanșatori
La copiii cu PANS/PANDAS crizele pot fi generate de o nouă infecție. De asemenea, stresul psihosocial (inclusiv bullying) este un factor declanșator. De aceea se recomandă o formă de școlarizare la domiciliu, măsură însoțită de respectarea regulilor de igienă de către toți membrii familiei. În același scop, este important să se evite locurile aglomerate.
La copiii cu PANS (non-streptococic), o infecție cu streptococi de grup A poate declanșa o criză de PANDAS. Invers, la copiii cu PANDAS, alte infecții pot genera crize de PANS.
Cei mai cunoscuți declanșatori sunt:
– Mycoplasma pneumoniae.
– Chlamydia pneumoniae.
– Streptococcus pneumoniae.
– Borrelia burgdorferi.
– Bartonella species.
– Staphylococcus aureus.
– Pseudomonas aeruginosa.
– Coxsackie virus.
– virusuri gripale.
– SARS-CoV-2.
– Epstein-Barr virus.
– Varicella Zoster virus.
– Herpes Simplex virus.
– enterovirusuri.
– substanțe chimice (glyphosate, agenți de curățare, compuși organici volatili, aditivi alimentari etc.).
Unele mucegaiuri produc micotoxine care pot afecta sistemul nervos. La copiii cu PANS/PANDAS, expunerea la aceste toxine poate agrava manifestările neuropsihiatrice. Anumite micotoxine, precum ochratoxin și trichothecenes pot traversa bariera hematoencefalică și pot afecta direct funcționarea creierului. [67]
Vaccinarea poate fi un declanșator PANS/PANDAS.
Un studiu publicat în 2023 pe un eșantion de 181 copii cu PANS/PANDAS care au primit vaccin anti-COVID-19, a arătat că 19% au raportat crize (reactivări) ușoare, iar 15% au raportat crize severe de PANS/PANDAS.
Siguranța noilor vaccinuri ar putea fi deosebit de relevantă pentru pacienții deja predispuși la dereglarea răspunsurilor imune, având în vedere mimetismul molecular al vaccinului și potențialul vaccinului cu ARNm de a activa mai multe cascade proinflamatorii. [30][1]
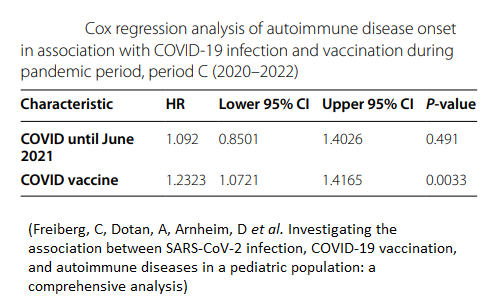
Programul de vaccinare COVID-19 al Israelului a fost implementat în etape. A început cu persoanele de 16 ani și peste în decembrie 2020, s-a extins la copiii de 12 ani în iunie 2021 și la cei de 5 ani în noiembrie 2021. Un studiu pe un eșantion pediatric din Israel (4596 pacienți cu boli autoimune) a arătat că infecția cu COVID-19 nu a crescut riscul de boli autoimune, însă vaccinările au prezentat un risc semnificativ crescut de dezvoltare a afecțiunilor autoimune cu peste 23%. Aceste rezultate sunt în concordanță cu literatura actuală, care stabilește o legătură cauzală între vaccin și dezvoltarea efectelor adverse pe termen lung, în special bolile autoimmune. Principalele mecanisme propuse pentru autoimunitatea indusă de vaccin în urma vaccinării cu vaccin anti-SARS-CoV-2 includ mimetismul molecular, generarea de autoanticorpi și rolul adjuvanților din vaccin. [18]
Vaccinurile pot declanșa boli imunologice. Vasculita IgA (purpura Henoch-Schönlein), cea mai frecventă vasculită sistemică la copii, este o vasculită cu complexe imune care afectează în principal vasele de dimensiuni mici. Poate apărea după infecții respiratorii sau digestive, dar poate fi indusă și de vaccinuri precum vaccinul antigripal sau DTP. [41]
Agresiunile fizice, chimice, biologice și psihologice la care este supusă o persoană au efect cumulativ și dau o rezultantă (total load).
Lauren Lee Stone, specialist în Nutriție și Toxicologie, ne spune: “Când văd copii în practica mea diagnosticați cu PANS/PANDAS, analizez toți factorii care au contribuit la boală. Da, PANDAS este declanșat de o infecție cu streptococ. Dar este mai mult decât atât. Privesc întreaga poveste a corpului copilului. Și lucrez pentru a elimina factorii de stres și a detoxifia încărcătura totală. Tratarea bolilor multifactoriale necesită o abordare multifactorială.” [58]
Caracterizare metabolomică
Studiile au pus în evidență un profil metabolic plasmatic unic la pacienții cu PANS, în mod semnificativ diferit de cel al copiilor sănătoși, ceea ce sugerează implicarea unor tipare specifice neurotransmisiei (triptofan, glicină, histamină/histidină), neuroinflamației și stresului oxidativ (glutamină, 2-hidroxibutirat și calea triptofan-kinurenină) în această patologie. [71]
PANS și disbioza intestinală
Microbiota intestinală și creierul se află într-o permanentă legătură bidirecțională (axa microbiotă-intestin-creier).
Dezechilibrul microbiotei orale și intestinale afectează capacitatea de modulare a inflamației și neuroinflamației. [37]
Unii copii cu PANS/PANDAS au disbioză intestinală cu o diversitate alfa scăzută, multe bacterii producătoare de histamină, bacterii LPS-pozitive (Citrobacter spp., Enterobacter spp., Escherichia spp., Klebsiella spp., Providencia spp., Pseudomonas spp., Serratia spp., Sutterella spp.) și tendință spre Sindromul Intestinului Iritabil, leaky gut, boli neurologice și autoimunitate.
Concluzii
PANS și PANDAS fac parte din categoria afecțiunilor inflamatorii multisistemice, mai degrabă decât să fie tulburări psihiatrice sau neuroinflamatorii izolate. În sindromul de activare mastocitară apar multe simptome neuropsihiatrice comune cu PANS/PANDAS. Studiile mai vechi indicau un debut brusc, dar acum știm că în multe cazuri debutul este subacut și poate fi trecut cu vederea sau interpretat greșit. Modelul activării microgliei prin agresiunea în două etape (two-hit model) este important pentru înțelegerea neuroinflamației și a diferențelor clinice. Studiile au pus în evidență un profil metabolic plasmatic și un tipar de disbioză intestinală în cele mai multe cazuri de PANS/PANDAS.
Tratarea acestor boli multifactoriale necesită o abordare multifactorială.
Cine este Ion Vlăducă?
Ion Vlăducă este statistician medical, antrenor de Psihologie Pozitivă, cercetător, matematician și programator. Este pasionat de Biostatistică, Bioinformatică și studiul axei microbiotă-intestin-creier.

Bibliografie
Akinosoglou K, Tzivaki I, Marangos M. Covid-19 vaccine and autoimmunity: awakening the sleeping dragon. Clin Immunol. 2021; 226:108721.
Andreou D, Steen NE, Mørch-Johnsen L, Jørgensen KN, Wortinger LA, Barth C, Szabo A, O’Connell KS, Lekva T, Hjell G, Johansen IT, Ormerod MBEG, Haukvik UK, Aukrust P, Djurovic S, Yolken RH, Andreassen OA, Ueland T, Agartz I. Toxoplasma gondii infection associated with inflammasome activation and neuronal injury. Sci Rep. 2024 Mar 4;14(1):5327. doi: 10.1038/s41598-024-55887-9. PMID: 38438515; PMCID: PMC10912117.
Aydin IH, Takçi E, Kadioğlu HH, Kayaoğlu CR, Tüzün Y, The variations of lenticulostriate arteries in the middle cerebral artery aneurysms. Acta Neurochir (Wien). 1996;138(5):555-9. doi: 10.1007/BF01411176. PMID: 8800331.
Behrens M, Hüwel S, Galla H-J, Humpf H-U (2015) Blood-Brain Barrier Effects of the Fusarium Mycotoxins Deoxynivalenol, 3 Acetyldeoxynivalenol, and Moniliformin and Their Transfer to the Brain. PLoS ONE 10(11): e0143640. https://doi.org/10.1371/journal.pone.0143640.
La Bella S, Scorrano G, Rinaldi M, Di Ludovico A, Mainieri F, Attanasi M, Spalice A, Chiarelli F, Breda L. Pediatric Autoimmune Neuropsychiatric Disorders Associated with Streptococcal Infections (PANDAS): Myth or Reality? The State of the Art on a Controversial Disease. Microorganisms. 2023; 11(10):2549. https://doi.org/10.3390/microorganisms11102549
La Bella, S., Attanasi, M., Di Ludovico, A., Scorrano, G., Mainieri, F., Ciarelli, F., Lauriola, F., Silvestrini, L., Girlando, V., Chiarelli, F., & Breda, L. (2023). Pediatric Autoimmune Neuropsychiatric Disorders Associated with Streptococcal Infections (PANDAS) Syndrome: A 10-Year Retrospective Cohort Study in an Italian Centre of Pediatric Rheumatology. Microorganisms, 12.
Bérubé MD, Blais N, Lanthier S. Neurologic manifestations of Henoch-Schönlein purpura. Handb Clin Neurol. 2014;120:1101-11. doi: 10.1016/B978-0-7020-4087-0.00074-7. PMID: 24365374.
Bratman, G. N., Hamilton, J. B., & Daily, G. C., The impacts of nature experience on human cognitive function and mental health. Annual Review of Psychology, 2015, 66, 537-563.
Castañeda S, Quiroga-Colina P, Floranes P, Uriarte-Ecenarro M, Valero-Martínez C, Vicente-Rabaneda EF, González-Gay MA. IgA Vasculitis (Henoch-Schönlein Purpura): An Update on Treatment. J Clin Med. 2024 Nov 4;13(21):6621. doi: 10.3390/jcm13216621. PMID: 39518760; PMCID: PMC11546386.
Catalano G, Houston SH, Catalano MC, Butera AS, Jennings SM, Hakala SM, Burrows SL, Hickey MG, Duss CV, Skelton DN, Laliotis GJ. Anxiety and depression in hospitalized patients in resistant organism isolation. South Med J. 2003 Feb;96(2):141-5. doi: 10.1097/01.SMJ.0000050683.36014.2E. PMID: 12630637.
Cherry JD, Olschowka JA, O’Banion MK. Neuroinflammation and M2 microglia: the good, the bad, and the inflamed. J Neuroinflammation. 2014 Jun 3;11:98. doi: 10.1186/1742-2094-11-98. PMID: 24889886; PMCID: PMC4060849.
Cui, G., Jun, S., Jin, X. et al. Concurrent activation of striatal direct and indirect pathways during action initiation. Nature 494, 238–242 (2013). https://doi.org/10.1038/nature11846.
Digitale E, Brain-scan abnormalities found in children with PANS, https://med.stanford.edu/news/all-news/2020/05/brain-scan-abnormalities-found-in-children-with-pans.html.
Esnafoglu E, Cırrık S, Ayyıldı S, Erdil A, Increased Serum Zonulin Levels as an Intestinal Permeability Marker in Autistic Subjects. The Journal of Pediatrics, Volume 188, 2017, 240 – 244, https://doi.org/10.1016/j.jpeds.2017.04.004
Etemadifar M, Abtahi S-H, Abtahi S-M, Case Report. Hemiballismus, Hyperphagia, and Behavioral Changes following Subthalamic Infarct. Case Reports in Medicine Volume 2012, Article ID 768580, doi:10.1155/2012/768580.
Frankovich J, Swedo S, Murphy T, Dale R, Agalliu D, Williams K, Daines M, Hornig M, Chugani H, Sanger T, Muscal E, Pasternack M, Cooperstock M, Gans H, Zhang Y, Cunningham M, Bernstein G, Bromberg R, Willett T, Brown K, Farhadian B, Chang K, Geller D, Hernandez J, Sherr J, Shaw R, Latimer E, Leckman J, Thienemann M, Clinical Management of Pediatric Acute-Onset Neuropsychiatric Syndrome: Part II—Use of Immunomodulatory Therapies. Journal of Child and Adolescent Psychopharmacology, Volume 27, Number 7, 2017 Mary Ann Liebert, Inc.Pp. 574–593DOI: 10.1089/cap.2016.0148574.
Frankovich J, Thienemann M, Pearlstein J, Crable A, Brown K, Chang K, Multidisciplinary Clinic Dedicated to Treating Youth with Pediatric Acute-Onset Neuropsychiatric Syndrome: Presenting Characteristics of the First 47 Consecutive Patients. Journal of Child and Adolescent Psychopharmacology, Volume 25, Issue 1, February 2015, Pages 38-47 Mary Ann Liebert, Inc. https://doi.org/10.1089/cap.2014.0081.
Freiberg, C, Dotan, A, Arnheim, D et al. Investigating the association between SARS-CoV-2 infection, COVID-19 vaccination, and autoimmune diseases in a pediatric population: a comprehensive analysis. Pediatr Rheumatol 23, 52 (2025). https://doi.org/10.1186/s12969-025-01093-4.
Gagliano A, Carta A, Tanca M, Sotgiu S, Pediatric Acute-Onset Neuropsychiatric Syndrome: Current Perspectives. Neuropsychiatric Disease and Treatment 2023:19 1221–1250.
Gao P, Chen Q, Hu J, Lin Y, Lin J, Guo Q, Yue H, Zhou Y, Zeng L, Li J, Ding G, Guo G. Effect of ultrawideband electromagnetic pulses on bloodbrain barrier permeability in rats. Mol Med Rep. 2020 Oct;22(4):2775-2782. doi: 10.3892/mmr.2020.11382. Epub 2020 Jul 28. PMID: 32945403; PMCID: PMC7453585.
Giedd J, et al. Case Study: Acute Basal Ganglia Enlargement and Obsessive-Compulsive Symptoms in an Adolescent Boy. Journal of the American Academy of Child & Adolescent Psychiatry, Volume 35, Issue 7, 913 – 915.
Haley M, Brough D, Quintin J, Allan S. Microglial Priming as Trained Immunity in the Brain. Neuroscience, 2019, 405, pp.47-54. 10.1016/j.neuroscience.2017.12.039. pasteur-02873942.
Haruwaka, K., Ikegami, A., Tachibana, Y. et al. Dual microglia effects on blood brain barrier permeability induced by systemic inflammation. Nat Commun 10, 5816 (2019). https://doi.org/10.1038/s41467-019-13812-z.
Huber JD, Witt KA, Hom S, Egleton RD, Mark KS, Davis TP, Inflammatory pain alters blood-brain barrier permeability and tight junctional protein expression. Am. J. Physiol. Heart Circ. Physiol 2001;280:H1241–H1248. PubMed: 11179069.
Huey E, Zahn R, Krueger F, Moll J, Kapogiannis D, Wassermann E, Grafman J, A Psychological and Neuroanatomical Model of Obsessive-Compulsive Disorder. J Neuropsychiatry Clin Neurosci, 2008, 20(4): 390–408. doi:10.1176/appi.neuropsych.20.4.390.
Juncu V., Variabilitatea arterelor lenticulostriate şi importanţa lor clinică. Analele Ştiinţifice ale USMF „N. Testemiţanu” Nr. 1(12) / 2011 / ISSN 1857-1719, https://ibn.idsi.md/ru/vizualizare_articol/16039.
Kaur A , Chopra K , Kaur I , Rishi P, Salmonella Strain Specificity Determines Post-typhoid Central Nervous System Complications: Intervention by Lactiplantibacillus plantarum at Gut-Brain Axis. Frontiers in Microbiology Volume 11 – 2020, doi: 10.3389/fmicb.2020.01568.
Kumar A, Williams MT, Chugani HT. Evaluation of Basal Ganglia and Thalamic Inflammation in Children With Pediatric Autoimmune Neuropsychiatric Disorders Associated With Streptococcal Infection and Tourette Syndrome: A Positron Emission Tomographic (PET) Study Using 11C-[R]-PK11195. Journal of Child Neurology. 2014;30(6):749-756. doi:10.1177/0883073814543303.
Lam M., Wing Y. Mental Morbidities and Chronic Fatigue in Severe Acute Respiratory Syndrome Survivors: Long-term Follow-up. Arch Intern Med Published Online: 2009;169;(22):2142-2147. doi:10.1001/archinternmed.2009.384.
LaRusso MD, Abadia CE. Symptom flares after COVID-19 infection versus vaccination among youth with PANS/PANDAS. Allergy Asthma Proc. 2023 Sep 1;44(5):361-367. doi: 10.2500/aap.2023.44.230049. PMID: 37641227; PMCID: PMC10476495.
Lashnits E, Maggi R, Jarskog F, Bradley J, Breitschwerdt E, Frohlich F, Schizophrenia and Bartonella spp. Infection: A Pilot Case–Control Study.Vector-Borne and Zoonotic diseases, 2021, vol. 21, No. 6. https://doi.org/10.1089/vbz.2020.272.
Leon M, Jaba I, Cozma C, Albu E, Bahnea R, Mungiu O, Rezoluția inflamației – implicații farmacologice. Rev. Med. Chir. Soc. Med. Nat., Iaşi – 2011 – vol. 115, nr. 2.
Leonardi L , Perna C , Bernabei I , Fiore M, Ma M , Frankovich J , Tarani L, Spalice A, Pediatric Acute-Onset Neuropsychiatric Syndrome (PANS) and Pediatric Autoimmune Neuropsychiatric Disorders Associated with Streptococcal Infections (PANDAS): Immunological Features Underpinning Controversial Entities. Children 2024, 11, 1043. https://doi.org/10.3390/ children11091043.
Lopez-Castejon G, Brough D, Understanding the mechanism of IL-1b secretion. Cytokine & Growth Factor Reviews, Volume 22, Issue 4, 2011, 189-195, ISSN 1359-6101, https://doi.org/10.1016/j.cytogfr.2011.10.001.
Ma M, Masterson EE, Gao J, et al. Development of Autoimmune Diseases Among Children With Pediatric Acute-Onset Neuropsychiatric Syndrome. JAMA Netw Open. 2024;7(7):e2421688. doi:10.1001/jamanetworkopen.2024.21688.
Madokoro Y, Inoue H, Fujioka T, Mizuno M, Oomura M, Matsukawa N., [A case of unilateral chorea associated with cortical infarction with transient cortical and striatal hyperperfusion]. Rinsho Shinkeigaku. 2025 Apr 25;65(4):290-293. Japanese. doi: 10.5692/clinicalneurol.cn-002037. Epub 2025 Mar 22. PMID: 40128926.
Matera M, Biagioli V, Illiceto MT, Palazzi CM, Cavecchia I, Manzi A, Lugli S, Pennazzi L, Meocci M, Pedaci FA and Bertuccioli A (2025) Pediatric acute-onset neuropsychiatric syndromes and the gut-oral-brain axis: a narrative review of emerging microbiome-immune interactions and therapeutic perspectives. Front. Immunol. 16:1726630. doi: 10.3389/fimmu.2025.1726630
McKim, D., Weber, M., Niraula, A. et al. Microglial recruitment of IL-1β-producing monocytes to brain endothelium causes stress-induced anxiety. Mol Psychiatry 23, 1421–1431 (2018). https://doi.org/10.1038/mp.2017.64.
Oberholster L, Du Pasquier R, Mathias A, Exploring the role of brain-derived extracellular vesicles in viral infections: from pathological insights to biomarker potential. Front. Cell. Infect. Microbiol., 03 June 2024.Sec. Virus and Host
https://doi.org/10.3389/fcimb.2024.1423394.
Platt, MP, Bolding KA, Wayne C, Chaudhry S, Cutforth T, Franks K, Agalliu D, Th17 lymphocytes drive vascular and neuronal deficits in a mouse model of postinfectious autoimmune encephalitis. Proc. Natl. Acad. Sci. U.S.A. 117 (12) 67086716, https://doi.org/10.1073/pnas.1911097117 (2020).
Ramdani Y, Largeau B, Jonville-BeraA-P , Maillot F, Audemard-Verger A, COVID-19 Vaccination as a Trigger of IgA Vasculitis: A Global Pharmacovigilance Study. The Journal of Rheumatology Apr 2023, 50 (4) 564-567; DOI: 10.3899/jrheum.220629.
Robertson KR, Hall CD. Human immunodeficiency virus-related cognitive impairment and the acquired immunodeficiency syndrome dementia complex. Semin Neurol. 1992 Mar;12(1):18-27. doi: 10.1055/s-2008-1041153. PMID: 1615236.
Salvi V, Sozio F, Sozzani S, Del Prete A. Role of Atypical Chemokine Receptors in Microglial Activation and Polarization. Front Aging Neurosci. 2017 May 26;9:148. doi: 10.3389/fnagi.2017.00148. PMID: 28603493; PMCID: PMC5445112.
Schiro G, Shaik S, Laubitz D, Daines M, Rice S, Ghishan F, Kiela P. Gut microbiome alterations in Pediatric Autoimmune Neuropsychiatric Disorders Associated with Streptococcal Infections (PANDAS) suggests variation in the gut-brain axis and gut metabolic potential. Physiology, 2024 39:S1.
Šegždaitė G, Aliukonytė O, Pociūtė K. Neuropsychiatric Manifestations of Lyme Disease: A Literature Review of Psychiatric and Cognitive Impacts. Acta Med Litu. 2025;32(1):6-21. doi: 10.15388/Amed.2025.32.1.17. Epub 2025 Feb 18. PMID: 40641539; PMCID: PMC12239190.
Shabani F, Jadidi M, Esmaili M H, Sameni H R, Nazari H. Detrimental Effect of Mobile Phone Electromagnetic Field on Permeability of Blood-Brain Barrier. Middle East J Rehabil Health Stud.2020;7(3):e103714.https://doi.org/10.5812/mejrh.103714.
Solak H, Akkuş M, Avşar P, Relationship between serum oxidative stress and blood brain barrier parameters in patients with major depression. Journal of Psychiatric Research 2025, 190 , 25-31, https://doi.org/10.1016/j.jpsychires.2025.07.023.
Swedo S et al., Pediatric autoimmune neuropsychiatric disorders associated with streptococcal infections: Clinical description of the first 50 cases. Am. J. Psychiatry 155,264–271 (1998).
Taki El-Din Z, Iqbal H, Sharma A. Neurosyphilis-Induced Psychosis: A Unique Presentation of Syphilis With a Primary Psychiatric Manifestation. Cureus. 2023 Mar 13;15(3):e36080. doi: 10.7759/cureus.36080. PMID: 37056519; PMCID: PMC10094745.
Trifiletti R, Lachman HM, Manusama O, Zheng D, Spalice A, Chiurazzi P, et al. Identification of ultra-rare genetic variants in pediatric acute onset neuropsychiatric syndrome (PANS) by exome and whole genome sequencing. Sci Rep. (2022) 12:11106. doi: 10.1038/s41598-022-15279-3.
Wedervang-Resell K, Friis S, Lonning V, Smelror R, Johannessen C, Reponen E, Lyngstad S, Increased interleukin 18 activity in adolescents with early-onset psychosis is associated with cortisol and depressive symptoms. Psychoneuroendocrinology, Volume 112, 2020, 104513, ISSN 0306-4530, https://doi.org/10.1016/j.psyneuen.2019.104513.
Xu J, Liu R-J, Fahey S, Frick L, Leckman J, Vaccarino F, Duman R, Williams K, Swedo S, Pittenger C, Antibodies From Children With PANDAS Bind Specifically to Striatal Cholinergic Interneurons and Alter Their Activity. American Journal of Psychiatry, 2021 178:48–64. doi: 10.1176/appi.ajp.2020.19070698.
Xu J, Frankovich J, Liu RJ, Thienemann M, Silverman M, Farhadian B, Willett T, Manko C, Columbo L, Leibold C, Vaccarino FM, Che A, Pittenger C. Elevated antibody binding to striatal cholinergic interneurons in patients with pediatric acute-onset neuropsychiatric syndrome. Brain Behav Immun. 2024 Nov;122:241-255. doi: 10.1016/j.bbi.2024.07.044. Epub 2024 Jul 30. PMID: 39084540; PMCID: PMC11569416.
Xu X, Wu X, Zhu C, Zhang R, Jiaerken Y, Wang S, Hong H, Yu W, Li K, Zeng Q, Luo X, Yu X, Sun J, Zhang M and Huang P, Characterization of Lenticulostriate Arteries and Its Associations With Vascular Risk Factors in Community-Dwelling Elderly. Front. Aging Neurosci. 13:685571. doi: 10.3389/fnagi.2021.685571.
Yoon C-S. Natural Products in the Treatment of Neuroinflammation at Microglia: Recent Trend and Features. Cells. 2025; 14(8):571. https://doi.org/10.3390/cells14080571
Zakia H, Pradana K, Iskandar S (2023) Risk factors for psychiatric symptoms in patients with long COVID: A systematic review. PLoS ONE 18(4): e0284075. https://doi.org/10.1371/journal.pone.0284075.
Zheng J, Frankovich J, McKenna ES, Rowe NC, MacEachern SJ, Ng NN, Tam LT, Moon PK, Gao J, Thienemann M, Forkert ND, Yeom KW. Association of Pediatric Acute-Onset Neuropsychiatric Syndrome With Microstructural Differences in Brain Regions Detected via Diffusion-Weighted Magnetic Resonance Imaging. JAMA Netw Open. 2020 May 1;3(5):e204063. doi: 10.1001/jamanetworkopen.2020.4063. PMID: 32364596; PMCID: PMC7199120.
https://bettermedicine.ro/despre-pans-si-pandas-neuroinflamatii-cu-debut-brusc-la-copii
https://brainimmune.com/autoimmunity-inflammation-pans-pandas/
https://chandramd.com/wp-content/uploads/2021/11/Aman-Marya-Poster.pdf
https://drroseann.com/podcast/magnesium-and-pans-pandas-with-dr-darin-ingels/
https://ehtrust.org/wi-fi-wireless-radio-frequency-radiation-can-damage-the-blood-brain-barrier/
https://enviroproz.com/blog/the-effects-of-indoor-mold-on-children-with-pans-or-pandas/
https://www.pandasppn.org/research-library/metabolomic-characterization/
Treatment of Children with PANDAS PANS in Large Cohort of Italian Children | Fernanda Falcini, MD, PANDAS Network Official, https://www.youtube.com/watch?v=GLRwjbmTSio
Disclaimer
Informațiile prezentate în acest articol sunt destinate exclusiv scopurilor educative și informative. Acestea nu constituie un diagnostic medical, un tratament sau o recomandare terapeutică personalizată. Consultați întotdeauna un medic sau un specialist calificat înainte de a începe orice formă de tratament, dietă, supliment sau modificare a stilului de viață. Fiecare persoană este diferită, iar abordările care funcționează pentru un individ pot să nu fie potrivite pentru altul. Evaluarea și supravegherea profesională sunt esențiale.













2 comentarii. Leave new
Un articol de folos tuturor!
Mulțumim mult!
Mulțumesc și eu pentru interesul manifestat. Mulțumim Better Medicine Zenyth!