Scleroza multiplă este o boală autoimună care implică numeroși factori autoimuni, inflamatori, epigenetici și care ridică numeroase provocări atât pentru pacienți, cât și pentru specialiștii din domeniu.
Webinarul „Scleroza multiplă – O abordare integrativă”, din seria de webinarelor Zenyth Better Medicine, a adus în atenția noastră aspecte importante despre această afecțiune și modul în care pacienții își pot îmbunătăți calitatea vieții.
Maria Plăiaș, nutriționist certificat, practician de medicină funcțională, certificată la Institutul Dr. Kharazzian, lectorul webinarului, a prezentat informații esențiale atât pentru cei diagnosticați cu această boală, cât și pentru specialiștii care trebuie să îi ajute pe pacienți să gestioneze boala.
Ce este scleroza multiplă?
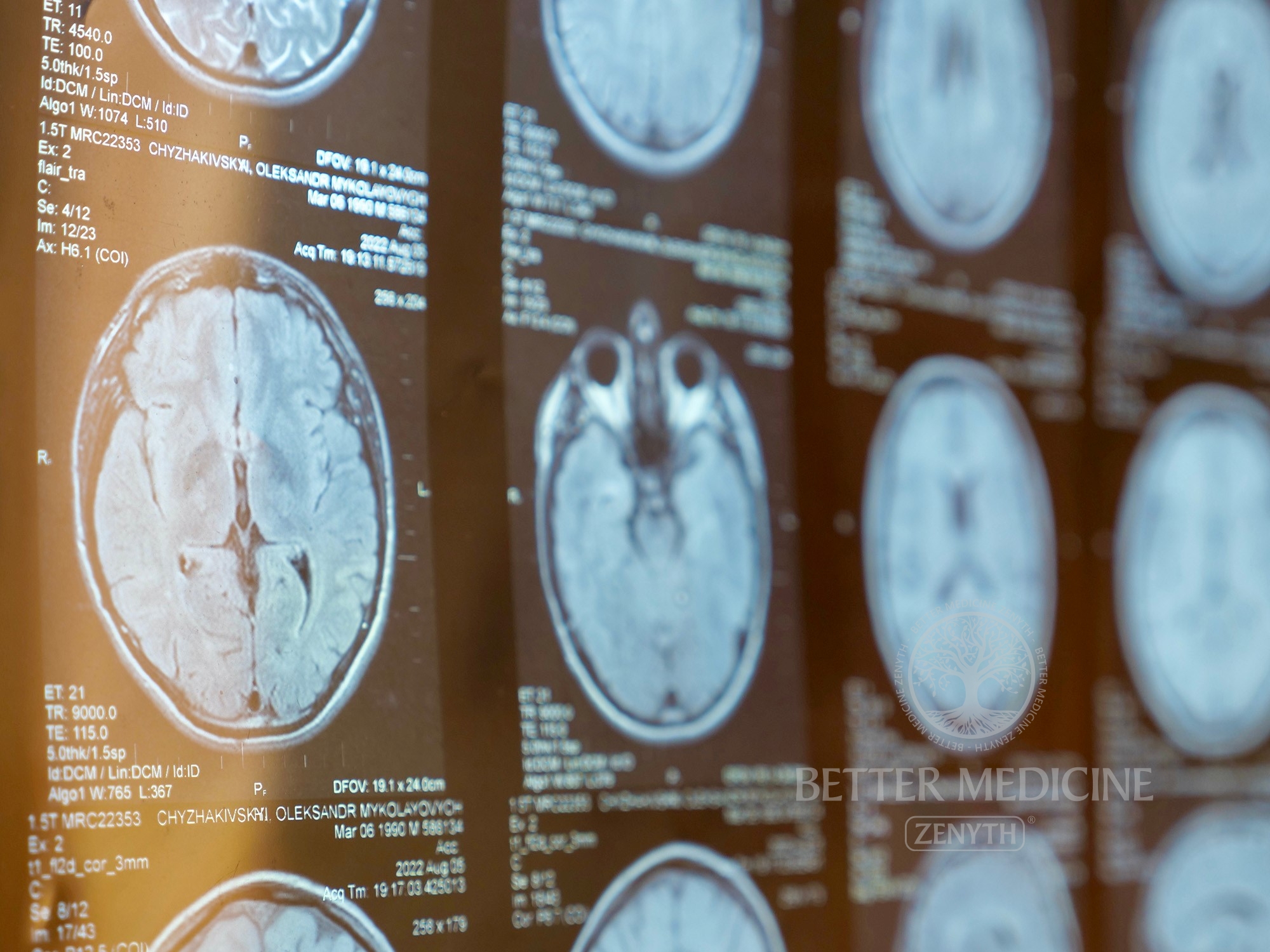
Scleroza multiplă (SM) face parte din afecțiunile demielinizante împreuna cu neuromielita optică (NMO) și este o boală neurologică autoimună care afectează mielina, învelisul protector al nervilor, la nivel de sistem nervos central, implicând creierul, nervul optic și măduva spinării, cu caracteristici imunologice și patologice distincte. Distrugerea mielinei implică întreruperea comunicării eficiente între creier și corp.
Teaca de mielină este o membrană protectoare care înfășoară o parte din anumite celule nervoase. Este un strat protector de grăsime (lipide) și proteine care acoperă secțiunea principală „corp” a unui neuron numit axon.
Boala e diagnosticată pe baza observațiilor clinice și testelor adjuvante, cum ar fi rezonanța magnetică a creierului și examinarea fluidului cerebrospinal și există un set de criterii bine definite care poartă numele de Criteriile McDonald din 2017, în baza cărora se pune diagnosticul corect.
Care sunt simptomele?
În funcție de zona în care apare atacul autoimun, simptomele pot varia, însă cele mai frecvente sunt:
- Oboseală.
- Înțepături și amorțeală, senzații de căldură în diferite părți ale corpului.
- Probleme cu vederea, vedere încețoșată sau chiar pierderea vederii.
- Dificultăți de atenție și memorie.
- Amețeli.
- Probleme de vorbire.
- Pierderea auzului.
- Tremurat al corpului.
- Dificultăți respiratorii.
Cu timpul, aceste simptome pot da naștere unor complicații secundare, inclusiv pierderea densității osoase sau chiar disfuncții ale vezicii urinare.
Tipologii ale sclerozei multiple
Pacienții pot fi grupați în 4 mari categorii în funcție de manifestarea bolii:
- SM recurent-remitentă: cea mai comună formă, afectând 85% dintre pacienți. Se manifestă prin puseuri recurente, urmate de luni sau ani de remisiune.
- SM secundar progresivă: apare la aproximativ 65% dintre pacienții care au prezentat inițial forma recurent-remitentă a bolii și care, în urma atacurilor, au suferit o deteriorare neurologică progresivă, cu sau fără perioade de remisiune minore sau perioade de platou. Perioada între debutul bolii și trecerea la forma secundar progresivă a acesteia este de aproximativ 19 ani. Această formă apare de regulă în jurul vârstei de 40 de ani.
- SM primar progresivă: apare la 10–20% dintre pacienți care nu au perioade de remisiune sau ameliorări dupa simptomele inițiale sau, daca au, acestea sunt ocazionale și prea puțin relevante.
- SM progresiv-recidivantă: o formă rară ce afectează mai puțin de 5% dintre pacienți. Este progresivă încă de la început, cu puseuri intermitente și simptome ce se agravează treptat. Nu există perioade de remisie.
Care sunt factorii de risc?
Au fost definiți anumiți factori care pot crește riscul de a dezvolta scleroză multiplă, astfel: vârsta (SM se poate declanșa la orice vârstă, cu debut în intervalul 20 – 40 de ani), sexul (femeile sunt mai predispuse de 2-3 ori mai mult decât bărbații la apariția formei de SM recurent-remisivă), antecedente familiale (există un risc mai mare în familiile în care unul dintre părinți sau frați a avut SM), infecțiile declanșate de anumite virusuri (cum ar fi Epstein-Barr, care provoacă mononucleoza infecțioasă), rasa (persoanele de etine albă, în special cele de origine nord-europeană, au cel mai mare risc de a dezvolta boala), clima (frecvență mai mare este în țările cu climă temperată, inclusiv în Canada, nordul Statelor Unite, Noua Zeelandă, sud-estul Australiei și Europa).
Un rol important pare să-l aibă vitamina D (niveluri scăzute ale vitaminei D și o expunere redusă la lumina soarelui se asociază cu un risc mai mare de SM), anumite boli autoimune (risc crescut la pacienții care asociază și alte afecțiuni autoimune, cum ar fi boala tiroidiană, anemia pernicioasă, psoriazisul, diabetul de tip 1 sau boala inflamatorie intestinală), fumatul (fumătorii sunt susceptibili să dezvolte scleroză multiplă recurent-remisivă).
Rolul celulelor microgliale
Într-un creier neinflamat, microglia are rol de curățare, adică se ocupă de eliminarea resturilor de neuroni morți pentru a reduce orice risc de inflamare. De asemenea, pot inhiba procese inflamatorii prin inducerea de apoptoză în celulele T invadatoare. Toate procesele astea au un rol anti-inflamator pentru creier.
Pe de altă parte, în creierul inflamat, microglia dezvoltă un rol de fagocitare excesiv și ajung să fagociteze și neuroni vii, ceea ce duce la pierderea capacității neuronale.
Aspecte imunologice în scleroza multiplă
Axa intestin – creier. Există 4 mecanisme ce au loc pe axa intestin – creier:
- Cel mai cunoscut e cel între inflamație și nervul vag. Inflamația generată de disbioza la nivel de intestin duce la inflamația neurologică, ceea ce reduce funcționalitatea nervului vag și înrăutățește funcția digestivă.
- Histamina și mastocitele. Prezența histaminei și a mastocitelor creează un circuit vicios de inflamație la nivel de intestin versus sistem nervos central.
- Activarea sistemului nervos simpatic. Împreună cu activare SNS are loc și o secreție de cortizol la nivelul glandelor suprarenale. Un singur eveniment stresant nu e inflamator, dar stresul cronic poate să ducă la o activare constantă a SNS inflamator.
- Polarizarea celulelor T si autofagie: 2 factori majori duc spre dominanța Th2: primul e țesutul epitelial din intestin care secretă citokine ce polarizează spre Th2 și al doilea este secreția de cortizol ca răspuns la activarea SNS ce are loc odată cu inflamația la nivel de SNC.
Mimetismul molecular apare când anticorpii nu se leagă de întreaga proteină, ci doar de o secvență proteică. Similaritatea dintre structurile de aminoacizi pot duce la confuzia sistemului imunitar și la producerea de anticorpi ce acționează încrucișat (mecanismul funcționează cu structuri proteice alimentare, dar și cu infecții sau substanțe chimice).
Despre protocolul Coimbra
Protocolul Coimbra este protocol clinic pentru tratarea bolilor autoimune, în special a sclerozei multiple și se bazează pe restabilirea unor niveluri sistemice adecvate de vitamina D, sub supravegherea unui medic calificat.
Cel care a dezvoltat acest protocol este Cicero Coimbra MD, PhD, neurolog și profesor la Universitatea Federală din São Paulo, Brazilia. Bazându-se pe literatura medicală actuală, el a descoperit că D3 are rol imunoreglator și stimulează producția de substanțe regenerative în creier, dovedindu-se o resursă terapeutică fundamentală.
Dr. Coimbra a început să prescrie vitamina D în doze de aprox 10.000 UI/zi pacienților cu SM si a văzut o îmbunătățire clinică remarcabilă la majoritatea pacienților săi. A crescut dozele mai mult, ajutându-se de teste de laborator pentru a reduce riscul de efecte secundare, precum excesul de calciu în sânge (hipercalcemie) sau în urină (hipercalciurie) sau pierderea masei osoase.
Din 2012 a fost atins nivelul dorit de eficacitate utilizând doze între 30.000 UI și 300.000 UI /zi.
Pentru a verifica doza fiecărui pacient în parte se folosește valoarea PTH (hormonul paratiroidian) deoarece atunci când valoarea PTH este menținută la cea mai inferioară limită normal se obține cel mai bun efect biologic al vitaminei D (PTH evaluează amploarea rezistenței la vitamina D). Dozele zilnice de vitamina D sunt crescute până la atingerea nivelului dorit de PTH și când se întâmplă acest lucru, rezistența la vitamina D este depășită și pacientul începe să beneficieze de puternicele sale efecte imunomodulatoare. Acest proces durează aproximativ 2 ani.
Aspecte epigenetice în scleroza multiplă
Epigenetica este ramură a geneticii care studiază modificările trăsăturilor fenotipice induse de mediu prin modificarea reversibilă a funcțiilor genelor, fără modificarea secvențelor ADN.
Epigenetica explică cum influențează mediul funcţionarea dinamică a genelor. Variațiile epigenetice sunt determinate de nutriție, infecții, noxe chimice, stres. Infecțiile, bolile alergice, afecțiunile maligne prezintă o semnificativă dimensiune epigenetică.
Au fost identificate mai mult de 200 variatii genetice sau polimorfisme care ar putea contribui la dezvoltarea sclerozei multiple. Printre aceste variante, multe implică metabolismul metioninei sau genele căii de metilare.
Cei mai importanți factori epigenetici în cazul SM sunt vitaminele liposolubile (D, A, K), acizii grași esențiali, metilarea, glutationul.
Cercetările au arătat că menținerea suficientă a vitaminei D în organism poate reduce riscul de scleroză multiplă (SM). Mai multe studii au arătat că persoanele care primesc mai multă expunere la soare și vitamina D în dieta lor sunt mai puțin susceptibile de a avea SM. Suplimentarea cu vitamina D este considerată o modalitate importantă de a modifica riscul de boală.
Unele studii sugerează, de asemenea, că vitamina D poate aduce beneficii persoanelor care au deja SM și anume simptomele pot apărea mai rar și la o intensitate mai scăzută ceea ce ar putea îmbunătăți calitatea vieții.
Vitamina A sintetizată de astrocite contribuie în mod considerabil la dezvoltarea și formarea barierei hematoencefalice. De asemenea, vitamina A joacă un rol protectiv împotriva radicalilor liberi în leziunile de la nivelul barierei hematoencefalica.
Tot ea reduce expresia IL-6 la nivel de creier jucând rol de agent terapeutic în bolile neuroinflamatorii. Suplimentarea cu vitamina A a redus procesul de demielinizare la nivel de SNC în studii pe șoareci.
O altă vitamină foarte importantă pentru pacienții cu SM este vitamina K. S-a observat ca aceasta era de 3 ori mai scăzută în grupul SM decât în grupul de control. Nu au fost găsite corelații între nivelul de K2 și tipul de SM, dar valoarea scăzută a vitaminei K a fost asociată cu un număr crescut de atacuri pe an.
Rolul mitocondriilor în scleroza multiplă
Mitocondriile sunt organe care au rolul să genereze energia de care celula are nevoie ca să trăiască: convertesc nutrienții și oxigenul în energie, pe care o acumulează în celule sub formă de adenozin trifosfat (ATP) si pe care celulele îl folosesc pe post de combustibil.
Mitocondriile furnizează peste 90% din necesarul de energie al organismului nostru, dar au și roluri non-energetice, de sesizare a stimulilor din mediul înconjurător, de comunicare și semnalizare a lor.
De asemenea, influențează direct reglarea metabolică sistemică, funcția creierului, activarea imunitară și chiar rata de îmbătrânire și durata de viață.
Mitocondriile joacă un rol esențial în transformarea celulelor T naive în celule T efectoare.
Manipularea dietei si a mitocondriilor ar putea ajuta la echilibrarea sistemului imunitar. Există mai multe diete benefice în acest sens, printre care: dieta Swank și dieta Wahls.
Prezențe patogenice în scleroza multiplă
În cazul pacienților cu SM s-au găsit niveluri crescute de anticorpi împotriva tulpinilor de Acinetobacter, Pseudomonas aeruginosa, Mycobacterium avium, Epstein-Barr și HHV-6 (virus herpetic uman de tip 6).
Studiile epidemiologice au oferit dovezi convingătoare că SM este o complicație rară a infecției cu virusul Epstein-Barr (EBV), un herpesvirus care infectează peste 90% din populația globală. Această legătură a fost mult timp suspectată, deoarece riscul de SM crește semnificativ după mononucleoza infecțioasă (infecție primară simptomatică cu EBV) și cu titruri mari de anticorpi la antigeni specifici EBV. Cu toate acestea, abia în 2022 = un studiu longitudinal a demonstrat că riscul de SM este minim la persoanele care nu sunt infectate cu EBV și că acesta crește de peste 30 de ori după infecția cu EBV.
Cum influențează metalele grele evoluția bolii?

Dintre factorii de mediu, metalele grele pot juca un rol important în SM. Având în vedere toxicitatea ridicată și persistența pe termen lung a metalelor grele din ecosistem, acestea au cel mai dăunător efect asupra sănătății umane dintre diferitele poluări ale mediului, inclusiv expunerea la lumina soarelui, bacterii, virusuri și xenobiotice, cum ar fi substanțele chimice, medicamentele și metalele.
Aceste substanțe își exercită toxicitatea prin diferite mecanisme, inclusiv formarea de radicali liberi, distrugerea membranei celulare, inhibarea enzimatică și inducerea autoimunității. Mai mult, studiile au arătat că expunerea la aceste neurotoxice intensifică progresia SM.
Principalele metale care au fost asociate cu SM sunt: aluminiu, arsenic, bor, cadmiu, crom, gadolinium, mercur.
Sănătatea tractului intestinal în scleroza multiplă
Așa cum am văzut încă de la începutul webinarului, există o legătură între intestin și creier și această conexiune este ca o stradă pe care se circulă în ambele direcții: sistemul nervos enteric conectează sistemul digestiv de creier prin intermediul nervului vag.
Multe studii științifice relevă o legătură semnificativă între microbiota intestinală umană, obiceiurile alimentare și dezvoltarea bolilor cronic-degenerative; prin urmare, modificările compoziției și funcției microbiotei pot fi însoțite de diferite mecanisme inflamatorii cronice.
Există o cascadă imunologică cauzată de disbioză. Disbioza intestinală poate duce la producția epitelială de NFkB în tractul intestinal, iar prezența NFkB la nivel epitelial va duce la cresterea valorilor de IL-1beta care va duce la inflamație sistemică mediată de IL-1beta care va produce neuroinflamație.
Neuroinflamația va cauza reducerea activității la nivel de cortex prefrontal și asta duce la o comunicare mai redusă a cortexului cu trunchiul cerebral și la reducerea funcționalității nervului vag care, în final, duce la pierderea efectului antiinflamator pe care îl are asupra ficatului, splinei și intestinului subțire. Când pierdem acest efect antiinflamator, se consolidează procesul inflamator originar.
Pe de altă parte, odată cu reducerea funcționalității nervului vag se reduce și motilitatea intestinală și în acest caz e posibil să apară suprapopularea bacteriană a intestinului subțire (SIBO).
Rolul stresului și traumei

Un alt factor important în patogeneza bolilor autoimune îl reprezintă stresul. Atunci când vorbim de stres trebuie să vorbim și de traumă, mai ales de o predispoziție care are loc de la o vârstă tânără și anume Adverse Childhood Experience(ACE). Există o categorie de 10 experiențe care fac parte din trauma cu T mare: abuz emoțional, sexual sau fizic; neglijare fizică sau emoțională; pierderea unui părinte prin divorț; violență domestică; părinte cu boli mintale (depresie); părinte cu adicții de alcool sau droguri sau care a fost la închisoare. Pentru fiecare punct ACE crește cu 20% riscul de a dezvolta o boală autoimună.
Tensiunea și trauma sunt atât psihologice, cât și fizice și le putem elibera prin abordări somatice TRE (Trauma/Tension Release Exercises ajută corpul să elibereze tiparele musculare profunde de stres, tensiune și traumă) sau Somatic Experiencing (abordare somatică ce ne oferă un cadru de siguranță pentru a evalua situația în care clientul e “blocat” sau “inghețat” emoțional, care ne permit să urmărim răspunsurile corpului pentru a facilita procesul de reglare a sistemului nervos autonom și a restabili comunicarea corp-minte-emoții, oferind instrumente clinice pentru a rezolva aceste stări fiziologice care stau la baza multor simptome ale traumei).
Dieta și stilul de viață în scleroza multiplă

Dieta joacă un rol esențial în managementul SM. Deși nu există o dietă oficială pentru SM, există recomandări care ajută la reducerea inflamației și îmbunătățesc starea generală a organismului.
Printre aceste recomandări se numără și eliminarea glutenului, deoarece foarte multe studii au concluzionat că au găsit valori mari ale anticorpilor anti-gliadină în cazul persoanelor cu SM. De asemenea există și multe alimente care dau reactivitate încrucișată cu glutenul, precum multe proteine din lactate, sorg, drojdie, porumb, mei, ovăz.
Există mai multe diete care se recomandă în caz de SM. Dintre acestea, în cadrul webinarului Maria a vorbit despre: dieta Swank, dieta mediteraneană, dieta Paleo, dieta ancestrală, protocolul Wahls, fasting-ul. Factorul comun al acesor diete este reglarea microbiotei intestinale.
Ea a tras un semnal de alarmă asupra consumului de sare care a fost asociat cu declanșarea Th17 și promovează inflamația țesuturilor.
De asemenea, fumatul are un imapct foarte grav asupra sclerozei multiple și ar trebui să fie eliminat.
Pe lângă dietă, stilul de viață are o mare importanță în gestionarea SM. Mișcarea ajută la repararea creierului, mitocondriei, la reconectarea celulelor în creier și este absolut nevoie de ea.
Alte abordări integrative sunt crioterapia și terapia hiperbarică, dar studiile nu sunt încă finalizate.
Nutrienți și alte suplimente în scleroza multiplă
Există 3 categorii de suplimente care pot să ajute:
- Cu rol imunologic: oximatrina, baicalin, berberina.
- Utile în remielinizare: vitaminele A, D, K, nigella sativa.
- Alte suplimente de suport: LDN (naltrexonă în doză scăzută), ulei CBD (ulei de canabis).
Pe scurt..
Având în vedere că sunt o serie de necunoscute în ceea ce privește cauzele care duc la declanșarea sclerozei multiple, nu există moduri concrete prin care această boală se poate preveni. Totuși, este recomandat un stil de viață sănătos, bazat pe o dietă echilibrată și pe un program cu ore suficiente de somn și cu suplimente personalizate.
Scleroza multiplă afectează persoana bolnavă din toate punctele de vedere: medical, social, personal, profesional. De aceea, aceasta trebuie să se adapteze, să accepte schimbările prin care corpul va trece și să îl susțină, astfel încât interacțiunile cu societatea și cu cei din jur să fie cât mai puțin incomode.