Rezistența la insulină a devenit o frază tot mai folosită în ultima vreme și asta deoarece nivelul de conștientizare al importanței acesteia asupra calității vieții a devenit tot mai mare.
Webinarul Better Medicine Zenyth, cu tema „Rezistența la insulină. O abordare integrativă și funcțională“ partea a II-a, având-o lector pe dr. Camelia Ober, medic primar cardiolog la Institutul Inimii Cluj-Napoca, a evidențiat markerii și indecșii care pot fi folosiți pentru controlul glicemic și pentru rezistența la insulină, informații despre echilibrul glucozei și importanța celo 4 piloni: dietă, activitate fizică, managementul stresului și al somnului.
Cuprins
- Rezistența la insulină.
- Markeri pentru controlul glicemic.
- Indici de rezistență la insulină.
- Echilibrul glucozei.
- Cei 4 piloni ai sănătății metabolice: Dietă, Exerciții fizice, Managementul stresului, Somn.
Rezistența la insulină
Insulina este un hormon extrem de important în menținerea echilibrului glicemic, fiind chiar singurul hormon care determină scăderea glucozei din sânge pentru a asigura funcționarea normală a tututor organelor. Insulina este esențială pentru transportul intracelular al glucozei în țesuturile dependente de insulină, cum sunt mușchii, țesutul adipos și ficatul.
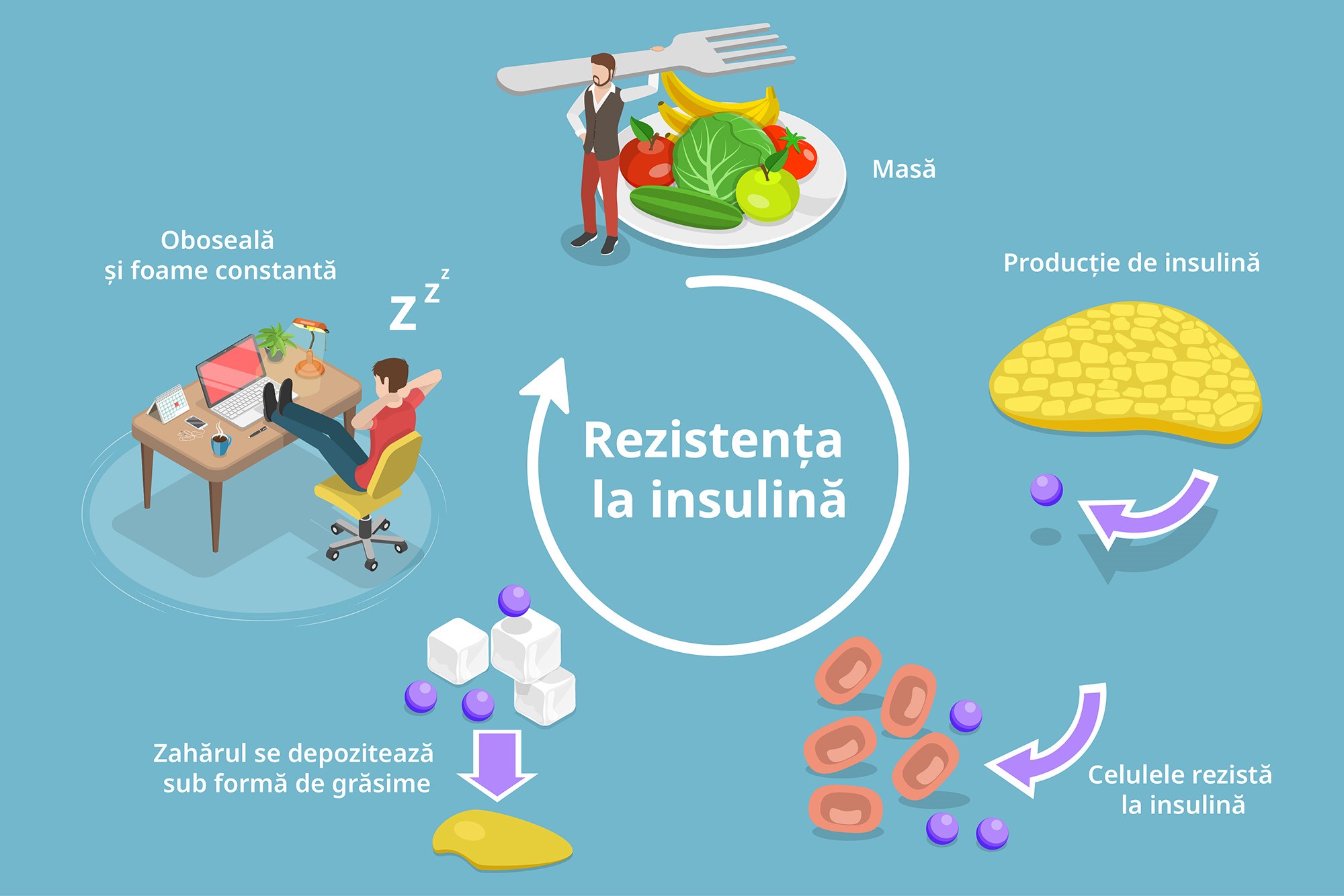
Rezistența la insulină este o tulburare metabolică cu mai multe fețe, caracterizată prin mecanisme fiziopatologice complicate, larg recunoscută ca un factor etiologic proeminent în diferite boli.
Rezistența la insulină este definită ca un efect atenuat al insulinei asupra homeostaziei glicemiei, în primul rând prin exportul mai puțin eficient al glucozei din sânge în mușchii scheletici, țesutul adipos și ficat.
Concentrațiile permanent crescute de insulină în sânge sunt adesea considerate ca o încercare de a depăși rezistența la insulină.
Markeri pentru controlul glicemic
Markerii tradiționali pentru controlul glicemic includ:
- Glicemia a jeun.
- Hemoglobina A1C (HbA1C).
- Glicemia postprandială (OGTT).
Standardul de aur pentru evaluarea controlului glicemic este HbA1C, care măsoară nivelul mediu al glicemiei pe o perioadă de aproximativ 3 luni.
Nivelurile de zahăr din sânge
| HbA1C (%) | Glicemia a jeun(mg/dl) | Testul de toleranță la glucoză orală | |
| DIABET | ≥ 6.5 | ≥ 126 | ≥ 200 |
| PREDIABET | 5.7 – 6.4 | 100 – 125 | 140 – 199 |
| NORMAL | 5 | ≤ 99 | ≤ 139 |
Indici de rezistență la insulină
Rezistența la insulină a fost evaluată inițial utilizând testul de supresie pancreatică, tehnica de clamp euglicemic hiperinsulinemic (TCEH) sau modelul minim de aproximare a metabolismului glucozei.
Cu toate acestea, aceste metode sunt invazive, complicate, costisitoare și dificil de utilizat clinic. Din aceste motive, au fost dezvoltați indici care măsoară rezistența la insulină.
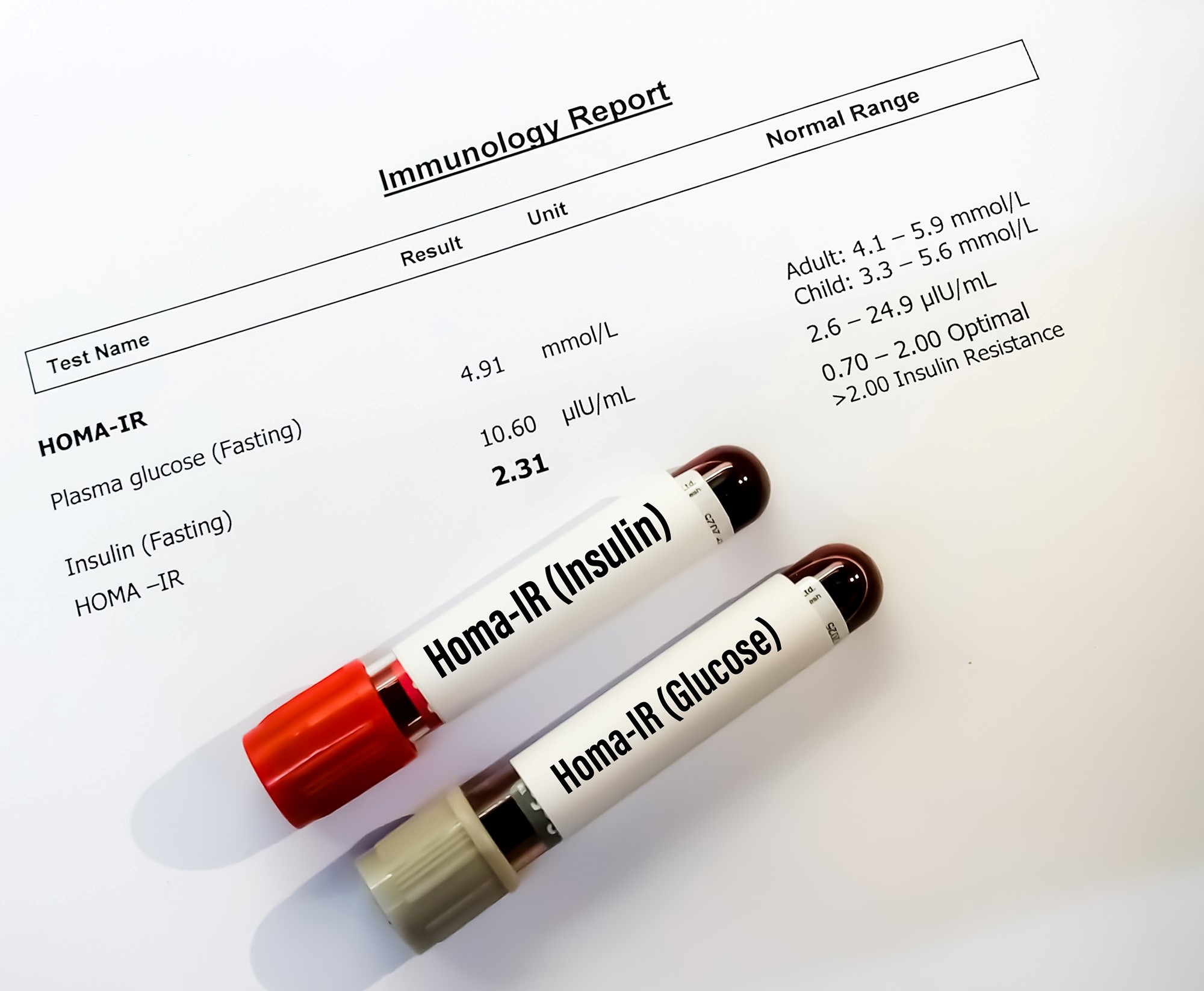
Indicele HOMA (normal <2) reflectă rezistența la insulină în stare de post (în principal rezistența la insulină în ficat). Acesta este derivat din produsul concentrațiilor plasmatice de glucoză și insulină a jeun.
Indicele Matsuda reflectă sensibilitatea la insulină în starea postprandială (în principal sensibilitatea la insulină în țesuturile periferice). Indicele Matsuda de sensibilitate la insulină conține glucoza plasmatică a jeun FPI (indicele rezistenței hepatice la insulină) și glucoza plasmatică medie înmulțită cu insulina plasmatică medie în timpul testului OGTT-oral de toleranță la glucoză (indicele rezistenței musculare la insulină).
De asemenea, au fost dezvoltați indici independenți de insulină, precum indicii lipidici.
Indicii lipidici includ:
- indicele de adipozitate viscerală (VAI).
- produs de acumulare de lipide (LAP).
- indicele de trigliceride și glucoză (TyG) – acesta poate anticipa boli care rezultă din rezistența la insulină.
Având în vedere că țesuturile adipoase secretă citokine inflamatorii, adipokine și specii reactive de oxigen, contribuind la o varietate de probleme metabolice, indicele TyG împreună cu parametrii de obezitate, cum ar fi IMC (indicele de masă corporală) și WC (circumferința taliei) ar putea fi indicatori mai buni ai rezistenței la insulină decât indicele TyG singur.
Combinația dintre IMC și TyG este un marker care poate fi folosit pentru idenficarea precoce a rezistenței la insulină.
Un alt paramentru care poate fi folosit este raportul TG/HDL.
TG/HDL-C >3 este capabil să identifice rezistența la insulină și riscul cardiometabolic crescut, inclusiv dezvoltarea diabetului zaharat de tip 2 la populații de diferite vârste.
Raportul TG/HDL a fost folosit ca surogat pentru LDL-C cu densitate mică și rezistența la insulină și a prezis boala coronariană în mod independent.
Echilibrul glucozei
Nivelurilor crescute cronice de glucoză din sânge asupra celulelor și țesuturilor, ca urmare a rezistenței la insulină, determină un efect toxic.
Surplusul metabolic reprezintă supraabundența de substraturi energetice (glucoză sau lipide) în raport cu cererea de energie celulară, care generează stres metabolic și, în general, are ca rezultat creșterea în greutate și stresul și/sau deteriorarea mitocondrială.
Disfuncția mitocondrială, stresul oxidativ și inflamația reprezintă consecințe celulare interconectate ale efectului hiperglicemic pe care hormonii de stres îl exercită asupra sistemelor de organe periferice.
Este important să ne gândim că aceste etape incipiente în care modificările sunt subtile sunt momentul potrivit de a interveni, astfel putând să oprim evoluția bolii.
Sindromul metabolic se regăsește cel mai mult în rândul celor care trăiesc sub presiune psihosocială sau în stres cronic.
Situațiile care declanșează răspunsuri la stres în zilele noastre sunt din ce în ce mai multe. Acești factori de stres sunt adesea de natură psihologică (de exemplu, lucrând pentru un șef autoritar sau îngrijirea unui membru al familiei care este grav bolnav etc). Ca urmare, răspunsul la stres poate deveni mai răspândit și mai puternic, sau chiar poate deveni cronic.
De asemenea, somnul jocă un rol foarte important în managementul sindromului metabolic. Tulburările de somn și perturbarea tiparelor diurne modifică nivelul de cortizol, care apoi provoacă rezistență la insulină și afectează reglarea glucozei.
Cei patru piloni ai sănătății metabolice
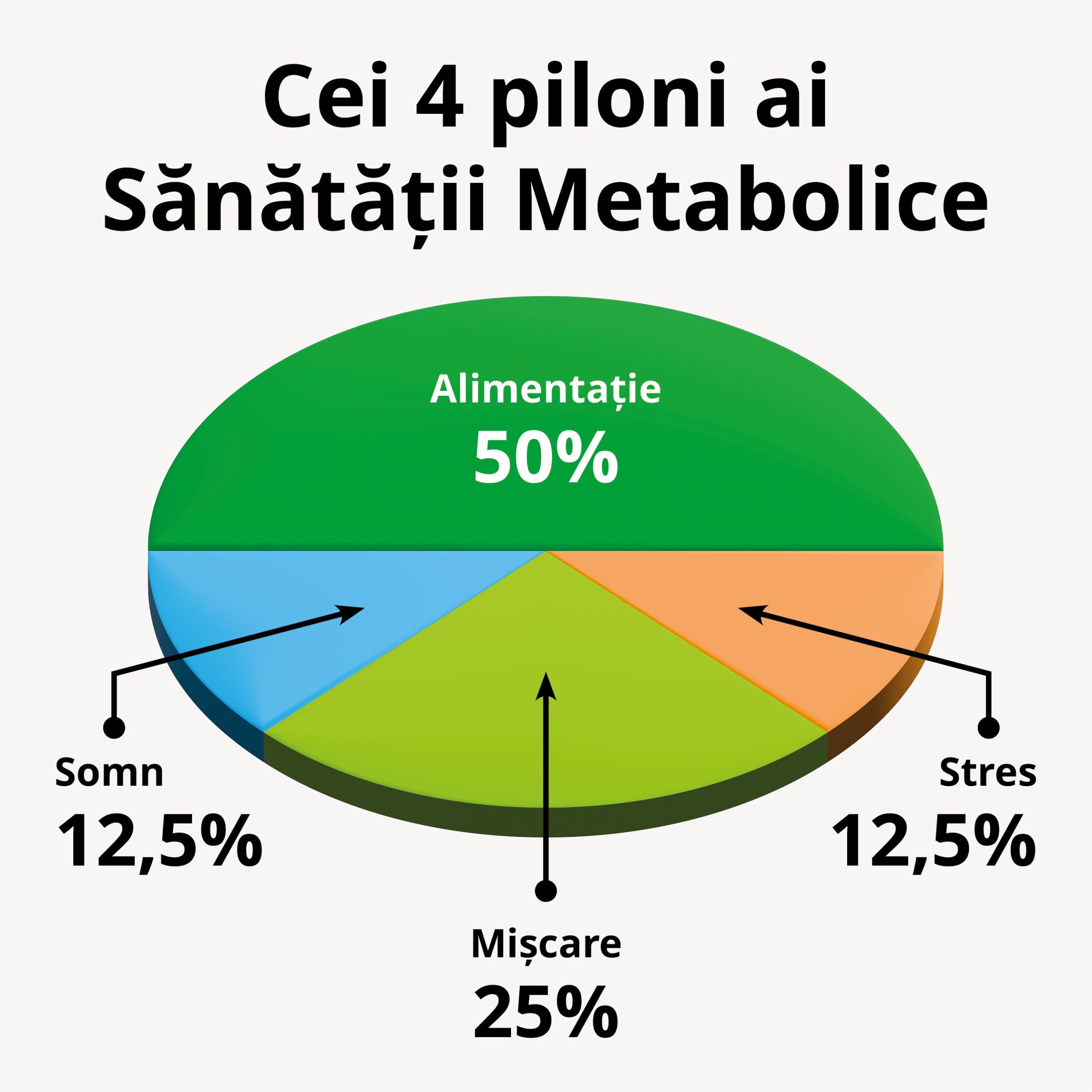
Pentru a inversa sau cel puțin pentru a încetini ritmul de dezvoltare a diabetului zaharat de tip 2 avem la dispoziție două mijloace importante:
- schimbarea stilului de viață, care include adoptarea de obiceiuri nutriționale sănătoase și practicarea de exerciții fizice regulate.
- medicamente/suplimente care pot:
- reduce glicogenoliza, gluconeogeneza;
- scade absorbția glucozei din intestin.
- Dieta și rolul ei în sănătatea metabolică
Dieta este considerată piatra de temelie în prevenirea și tratamentul tulburărilor legate de metabolismul glucozei și a rezistenței la insulină, iar alimentele au efecte majore asupra glicemiei postprandiale și asupra sănătății fizice generale.
Efectele insulinemice ale alimentelor pot fi relevante pentru tratamentul și prevenirea creșterii în greutate, a diabetului zaharat non-insulino-dependent și a complicațiilor asociate.
Alimentele diferite, dar care conțin cantități egale de carbohidrați, pot produce o gamă largă de răspunsuri la nivelul glucozei din sânge.
Metoda indicelui glicemic (IG) a fost dezvoltată pentru a clasifica alimentele în funcție de măsura în care acestea cresc concentrația de glucoză din sânge.
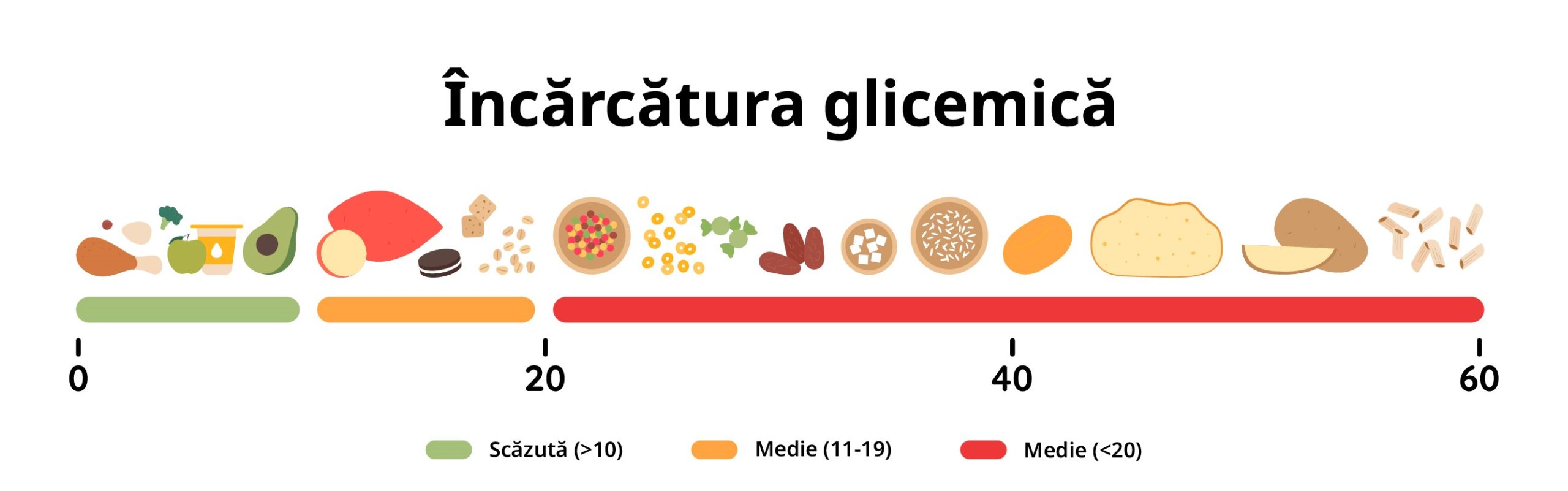
Mai importantă decât indicele glicemic este încărcătura glicemică.
În ceea ce privește tipul de carbohidrați, indicele glicemic (IG) descrie modul în care alimentele rapide specifice cresc glicemia (și, prin urmare, insulina) în cele 2 ore după consum.
Încărcarea glicemică (GL, produsul multiplicativ al cantității de carbohidrați și GI) este cel mai bun predictor unic al nivelurilor de glucoză din sânge postprandială, explicând până la 90% din varianță.
O valoare a încărcăturii glicemice de 10 sau mai puțin este considerată scăzută, 11-19 este considerată medie și 20 sau mai mult este considerată ridicată. Încărcătura glicemică va determina cantitatea de insulină pe care alimentul respectiv o va antrena.
O dietă bogată în carbohidrați:
- produce hiperinsulinemie postprandială.
- promovează depunerea de calorii în celulele adipoase, în loc de oxidare în țesuturile slabe.
- predispune la creșterea în greutate prin foame crescută, încetinirea ratei metabolice sau ambele.
Nu doar carbohidrații sunt stimuli pentru secreția de insulină, ci și alimentele bogate în proteine.
Alimentele bogate în proteine sau adăugarea de proteine la o masă bogată în carbohidrați pot stimula o creștere modestă a secreției de insulină, fără a crește concentrația de glucoză din sânge.
Iar adăugarea unei cantități mari de grăsimi la o masă bogată în carbohidrați crește secreția de insulină, chiar dacă răspunsurile la glucoza din plasmă sunt reduse.
Dacă nu abordăm problema pe termen lung a rezistenței la insulină, atunci nu vom putea arde eficient grăsimile. Dacă nivelurile ridicate de insulină ne blochează accesul la depozitele de grăsime, atunci aproape toată energia noastră trebuie să provină din alimente.
Din punct de vedere practic și din punct de vedere al impactului asupra organismulul este important să consumăm cea mai mare cantitate de hidrați de carbon la prânz.
De asemenea, este important de reținut că ceea ce dă semnalul de dimineață (micul dejun) are un rol foarte important asupra a ce face organismul cu mesele următoare. Deci, este important ca la micul dejun să nu consumăm glucide rapid absorbabile, dulciuri, tocmai pentru a evita acest răspuns inițial exagerat de insulină și pentru a preveni hipoglicemiile ulterioare și consumul excesiv de alimente.
Mai mult, trebuie să ținem cont și de faptul că există un ritm circardian și o sensibilitate diferită a țesuturilor de-a lungul zilei, cel mai prompt răspuns la insulină este de dimineață și spre prânz, iar spre seară se atenuează această sensibilitate la insulină în mod fiziologic.
Strategia alimentară pentru rezistența la insulină
Există mai multe strategii care pot ajuta la controlul rezistenței la insulină, printre care:
- O strategie alimentară cheie pentru tratarea hiperglicemiei postprandiale, hiperinsulinemiei și rezistenței la insulină este consumul de alimente și mese care diminuează fluctuațiile glucozei, cunoscute că induc stresul oxidativ și deteriorarea celulelor.
- O altă strategie importantă de luat în considerare este consumul de alimente și mese care induc o încărcătură glicemică mai scăzută și întârzie golirea gastrică, ducând astfel la scăderea necesarului de insulină și variații postprandiale de glucoză și pot reduce, de asemenea, foamea și dorința de a mânca.
- Un studiu care a utilizat monitorizarea continuă a glucozei la subiecții cu diabet zaharat de tip 2 a arătat că, pentru atingerea unor vârfuri mai mici de glucoză de 24 de ore, este mai bine să se consume cel puțin jumătate din cantitatea de carbohidrați la ora prânzului și să se evite consumul unor cantități semnificative de carbohidrați dimineața (la micul dejun) sau la masa de seară.
- Secvența meselor joacă un rol important în răspunsurile glicemice postprandiale. Există unele dovezi care sugerează că dacă consumi înainte de masă nutrienți precum apă, grăsimi, proteine sau fibre ca „preîncărcări”, întârzie viteza de absorbție postprandială a glucozei din intestinul subțire și atenuează secreția de insulină și nivelurile oscilante de glucoză.
- Exercițiile fizice după masă s-au dovedit a avea un impact pozitiv asupra glicemiei postprandiale. Momentul optim de timp pentru a deveni activ este cât mai curând posibil în faza postprandială timpurie (0–29 min după masă). Sunt suficiente 20 min de mers alert pentru a impacta glucoza (60-70% din glicemia postprandială este captată de mușchi în timpul exercițiului fizic).
Micronutrienții
Micronutrienții au, de asemenea, un rol foarte important în managementul rezistenței la insulină. Printre cei mai importanți se numără:
- Zincul pare a fi important în biosinteza și secreția insulinei.
- Deficiența de crom a fost asociată cu intoleranța la glucoză și rezistența la insulină (ionul de crom este transportat în fluxul sanguin prin transferină).
- Acumularea de fier este asociată cu afectarea sensibilității la insulină și diabet zaharat de tip 2 și cu caracteristici ale sindromului metabolic.
- Suplimentele de tiamină sunt necesare pentru a îmbunătăți funcția mitocondrială, deoarece derivații acestui micronutrient esențial funcționează ca coenzime ale multor enzime esențiale din mitocondrie.
- Vitamina E este importantă ca antioxidant, pentru a proteja biomembranele celulelor noastre și organele asociate.
- Suplimentarea cu coenzima Q10 poate îmbunătăți controlul glicemic printr-un efect direct asupra funcției mitocondriale
- Quercetina a fost raportată pe scară largă pentru efectul său favorabil asupra biogenezei mușchilor scheletici și mitocondriilor, precum și pentru funcționarea prin activarea axei SIRT1-AMPK-PGC 1α.
- S-a demonstrat că resveratrolul contracarează efectul dăunător al unei diete bogate în grăsimi.
- Mio-inozitolul inhibă absorbția duodenală a glucozei și reduce creșterea glicemiei printr-o afinitate competitivă pentru același sistem de transport.
- Un nivel scăzut de magneziu poate contribui la hiperinsulinemie și rezistență la insulină.
- Berberina reduce nivelul glicemiei prin reducerea sintezei glucozei în ficat (activarea enzimei protein-kinază – AMPK) și prin reducerea absorbției din intestin.
- Suplimentarea cu vitamina D3 poate îmbunătăți controlul glicemiei și poate reduce rezistența la insulină.
Exercițiul fizic și efectul său asupra glicemiei postprandiale
O mare parte a populației globale acumulează până la 16 ore de sedentarism zilnic și se află aproape permanent în stare de hrănire din cauza consumului frecvent de alimente.
Chiar și pentru oamenii sănătoși, nivelurile oscilante ale glicemiei rezultate sunt un factor de risc relevant pentru bolile inflamatorii de grad scăzut (inclusiv diabet zaharat de tip 2, boală hepatică grasă fără alcool și artrită reumatoidă) și bolile cardiovasculare.
Pentru pacienții cu diabet zaharat de tip 2 bine controlat, hiperglicemia postprandială este considerată a avea cel mai mare impact negativ asupra controlului glicemic pe termen lung, așa cum este indicat de nivelurile crescute de hemoglobină glicata (HbA1c).
În consecință, atenuarea variațiilor mari ale glicemiei induse de masă are un impact major asupra minimizării riscului pentru aceste boli asociate stilului de viață și asupra optimizării managementului zahărului din sânge la pacienții cu diabet zaharat de tip 2.
Puncte cheie:
- Exercițiile fizice au un impact benefic asupra glicemiei postrandiale dacă sunt făcute cât mai repede după masă.
- Cu cât intervalul între masă și exercițiul fizic este mai mare, cu atât scade impactul acestuia.
- Pentru persoanele care nu au timp să facă exerciții fizice după fiecare masă, perioade scurte de activitate fizică în jurul mesei pot fi eficiente pentru a reduce creșterea glicemiei postprandiale.
- Ridicarea de la birou pentru 2 de minute după fiecare 20 de minute poate fi de asemenea de ajutor.
Stresul și multiplele sale efecte
Rezistența la insulină este de obicei observată în stresul catabolic al bolilor severe, cu implicații pentru morbiditate și mortalitate.
Mecanismele includ:
- activarea axei hipotalamo-hipofizare suprarenale (HPA), care are ca rezultat creșterea hormonilor contrareglatori.
- efectele citokenelor inflamatorii.
- afectează semnalizarea receptorilor de insulină în mușchii scheletici, ficat și țesutul adipos.
Există mai multe metode de gestionare a stresului, printre care:
- Exercițiul fizic– intervenția cea mai accesibilă și care are cel mai mare impact asupra scăderii riscului de mortalitate. Nu este nevoie să mergi la sală, o plimbare de minimum 3-5 ori pe săptămână duce la o adaptare mai bună la stres. Antrenamentul fizic regulat crește efieciența energetică și scade riscul pentru orice boală cunoscută.
- Suportul social– poate antagoniza efectele expunerii la stres. Este important să menținem relațiile (față în față pe cât posibil) cu oamenii care ne sunt potriviți și cu care rezonăm.
- Tehnici de relaxare: meditație, yoga, rugăciune, emoții pozitive, muzică, capacitatea de a fi autentic.
Mai multe informații despre stres găsești aici.
- Somn și privarea de somn

Somnul este o nevoie fiziologică esențială a corpului uman, în egală măsură cu nevoia de hrană și hidratare. Deși somnul are un rol esențial în funcționarea fizică și psihică a omului, din păcate, stilul de viață modern nu ne ajută să ne bucurăm în mod organic de un somn liniștit și revigorant.
S-a raportat că lipsa acută de somn la adulții tineri sănătoși crește glicemia a jeun. Aceste efecte sugerează creșterea secreției hormonale contrareglatoare prin hiperexcitare, cu activarea axei hipotalamo-hipofizare suprarenale.
Există, de asemenea, dovezi că privarea cronică de somn poate avea un impact asupra insulinei și rezistenței la insulină. Privarea de somn este asociată cu scăderea concentrațiilor plasmatice de leptină, hormonul peptidic adipocitar care reglează masa grăsime și apetitul, și concentrații crescute de grelină, care crește apetitul.
Concluzii
Intervențiile care construiesc autoeficacitatea în general și în gestionarea rezistenței la insulină, în special, cum ar fi dieta sănătoasă, somnul regulat și activitatea fizică regulată, promovează o sănătate mai bună și vor duce, de asemenea, la scăderea incidenței bolilor cronice majore asociate cu aceasta.
Rezistența la insulină este o afecțiune fiziopatologică maleabilă, cu mai multe ținte periferice și centrale pentru intervenție înainte ca „switch-ul” să declanșeze toxicitate ireversibilă excitatoare/inflamatorie.
Agenții farmacologici pot fi utili ca facilitatori, dar nu vor funcționa singuri!














1 comentariu. Leave new
Excelent!!!!!!