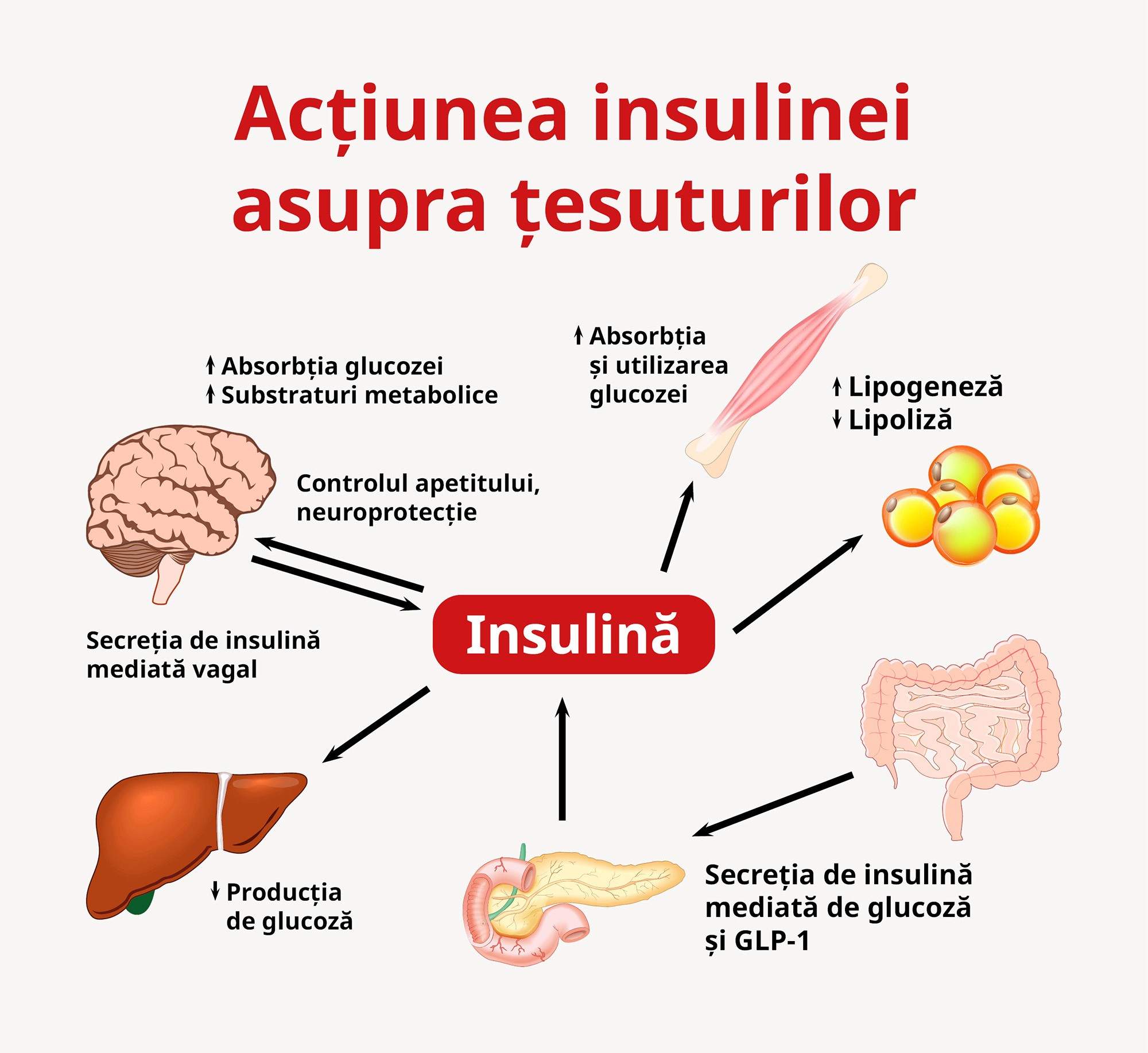
Deși creierul a fost considerat mult timp un organ independent de insulină, cercetări recente au arătat că insulina are efecte semnificative asupra lui, unde joacă un rol în menținerea homeostaziei glucozei și energetice. Pentru a evita rezistența periferică la insulină, creierul poate acționa prin răspunsuri hipoinsulinemice, menținând metabolismul glucozei și sensibilitatea la insulină în propriile limite. Cu toate acestea, rezistența la insulină a creierului se poate dezvolta din cauza factorilor de mediu.
Insulina are două funcții importante în creier: controlul aportului de alimente și reglarea funcțiilor cognitive, în special a memoriei. Defectele în semnalizarea insulinei în creier pot contribui la tulburări neurodegenerative. Rezistența la insulină poate afecta sistemul cognitiv și poate duce la stări de demență. În plus, procesele inflamatorii din hipotalamus, unde receptorii de insulină sunt exprimați la densitate mare, afectează sistemele locale de semnalizare și provoacă tulburări ale metabolismului glucozei și dezechilibre energetice.
Disfuncțiile cognitive

Organizația Mondială a Sănătății (OMS) definește demența ca „un sindrom în care există o deteriorare a funcției cognitive dincolo de ceea ce s-ar putea aștepta de la consecințele obișnuite ale îmbătrânirii biologice”. Conform celor mai recente estimări ale OMS, peste 55 de milioane de oameni trăiesc cu demență și aproximativ 10 milioane de cazuri noi se adaugă la acest grup în fiecare an. Deși demența afectează adesea persoanele în vârstă, nu este o consecință inevitabilă a procesului biologic de îmbătrânire. Demența nu afectează doar funcționarea fizică, economică și psihosocială a individului cu boală, dar are un impact enorm asupra îngrijitorilor, familiilor și societății și, prin urmare, stresează sistemele de sănătate în general.
Boala Alzheimer (o boală neurodegenerativă terminală cu progresie lentă, care poate rămâne asimptomatică timp de câteva decenii ) este cea mai frecventă formă de demență, prezentând peste 70% din toate cazurile, urmată de demența vasculară.
Pe lângă demența diagnosticată clinic, la pacienții diabetici au fost raportate disfuncții cognitive. Studiile recente încep acum să recunoască diabetul zaharat de tip 2, caracterizat prin hiperglicemie cronică și rezistență la insulină, ca factor de risc pentru boala Alzheimer și alte tulburări cognitive.
Din acest motiv, boala Alzheimer este denumită și „diabet al creierului” sau „diabet de tip 3”.
Studiile privind acțiunea insulinei au rămas, în primul rând, în domeniul bolilor periferice. Deși se știa că insulina reglează comportamentul de hrănire, creierul nu s-a considerat a fi o țintă majoră a acțiunii insulinei. Cu toate acestea, studiile încep să recunoască faptul că insulina joacă un rol în cogniție și neuroprotecție. Funcția creierului poate fi, de asemenea, afectată indirect de acțiunea insulinei asupra țesuturilor periferice. De exemplu, factorii circulanți în obezitate și diabet pot trece prin bariera hematoencefalică (BHE) și pot provoca disfuncții ale mai multor tipuri de celule cerebrale, inclusiv neuroni, astrocite și microglia. La periferie, pot fi generați și metaboliți insuficienți pentru a fi utilizați în creier, în condiții de rezistență la insulină.
Semnalizarea insulinei în creier
Se știe că insulina, produsă și eliberată de celulele β pancreatice, acționează în creier în plus față de țesuturile periferice. Insulina este ușor transportată prin BHE, printr-un proces mediat de receptori. Cu toate acestea, s-a sugerat că această cale de transport poate fi saturabilă, având în vedere că nivelurile de insulină din lichidul cefalorahidian (LCR) sunt corelate neliniar cu nivelurile de insulină plasmatică. Nivelurile de insulină din creier variază dramatic, hipotalamusul și bulbul olfactiv având concentrații de insulină mai mari decât nivelurile de insulină plasmatică.
Creierul este, de asemenea, o sursă de insulină, pe lângă insulina periferică, care este transportată prin BHE. S-a demonstrat că insulina este distribuită pe scară largă în creierul cadaveric uman prin radioimunotest.
Havrankov și colab. (1978) au fost primii care au raportat prezența rezistența la insulină în creierul șobolanului, pe baza studiilor de legare a insulinei. Legarea insulinei s-a dovedit a fi proeminentă în neocortex, zonele motorii accesorii ale ganglionilor bazali și cerebel. Studii ulterioare au arătat că receptorii de insulină sunt distribuiți abundent în tot creierul, în special în regiunile care reglează apetitul, funcția cognitivă, activitatea autonomă și olfacția. De asemenea, acești receptori sunt distribuiți selectiv în cortexul cerebral și cerebel. Astfel, studiile prezintă suficiente dovezi experimentale pentru a sugera că rezistența la insulină este exprimată în creier.
Semnalizarea insulinei și boala Alzheimer
S-a demonstrat că semnalizarea insulinei și leziunile Alzheimer au o relație bidirecțională. În timp ce rezistența la insulină a creierului joacă un rol în patogeneza Alzheimer, leziunile Alzheimer au, de asemenea, efecte dăunătoare asupra semnalizării periferice a insulinei și homeostaziei glucozei, ducând la un cerc vicios. Se raportează că pacienții cu Alzheimer au niveluri mai mari de insulină în sânge, un marker pentru rezistența periferică la insulină și o scădere a insulinei în lichidul cefalorahidian, în comparație cu pacienții sănătoși.
Nivelurile mai scăzute de insulină cerebrală și rezistența centrală la insulină se datorează parțial scăderii transportului de insulină în BHE și acumulării excesive de amiloid. În plus, creierul pacienților cu Alzheimer are niveluri scăzute atât de insulină, cât și de factori de creștere asemănători insulinei. Mediul din creier în timpul modificărilor neurodegenerative nu este propice semnalizării insulinei. De exemplu, neuroinflamația este o componentă cheie a patogenezei Alzheimer și se știe că citokinele interferează cu acțiunea insulinei. Un alt factor cauzal în creierul neurodegenerativ este stresul oxidativ care poate interfera și cu acțiunea insulinei.
Care este legătura dintre rezistența la insulină și Alzheimer?
Oamenii de știință cred că există câteva moduri prin care dificultățile cu controlul zahărului din sânge pot duce la probleme cu memoria și gândirea. Acestea sunt:
Inflamație și lezarea vaselor de sânge
Se știe că în caz de diabet zaharat crește riscul de atac de cord sau accident vascular cerebral, dar și că nivelurile ridicate de zahăr din sânge pot declanșa inflamația. Nimic din toate acestea nu este bun pentru vasele tale de sânge. Vasele deteriorate din creier ar putea duce la Alzheimer.
De asemenea, inflamația poate face celulele tale rezistente la insulină, mai ales dacă ești obez.
Comunicare nervoasă blocată
Nivelul ridicat de zahăr din sânge a fost legat de niveluri mai ridicate de proteine numite beta amiloid. Când acestea se adună, se blochează între celulele nervoase din creier și blochează semnalele, iar celulele nervoase care nu pot vorbi între ele sunt o trăsătură principală a Alzheimer.
Proteina Tau „încurcată”
Celulele tale mută în mod constant alimente și alte provizii de-a lungul căilor, precum șinele de cale ferată. O proteină numită Tau ajută aceste drumuri care intră, ies din/ și prin celule, să rămână în rânduri drepte.
Dar într-un creier cu Alzheimer, Tau se încurcă. Drumurile se destramă, iar celulele mor pentru că nu pot muta lucrurile acolo unde au nevoie.
O acumulare de Tau anormal duce la „încurcături” care provoacă leziuni celulare și inflamație, contribuind la simptomele bolii Alzheimer.
Ce poți să faci?
- Gestionează nivelul zahărului din sânge.
- Antrenează-te constant.
- Schimbă-ți stilul de viață.
- Monitorizează-ți greutatea.
- Renunță la alcool sau consumă-l cu moderație.
- Renunță la fumat.
- Scade nivelul de stres.
- Îmbunătățește calitatea somnului.
- Ține creierul ocupat cu activități intelectuale permanente.
Concluzii
Dovezi recente susțin afirmația că Alzheimer poate fi o boală metabolică a creierului, cu progresie lentă și numeroase studii demonstrează o legătură complicată între aceasta și sindromul metabolic. Persoanele cu caracteristici de sindrom metabolic, cum ar fi diabetul zaharat de tip 2 și obezitatea, au un risc mai mare de a dezvolta Alzheimer, în timp ce pacienții cu Alzheimer dezvoltă adesea hiperglicemie și rezistență la insulină.
Rezistența la insulină cauzată de semnalizarea afectată a insulinei este o caracteristică comună atât a sindromului metabolic, cât și a Alzheimer și reprezintă probabil legătura cheie între cele două boli.
Surse:
https://publications.aston.ac.uk/id/eprint/42233/1/ijms-22-00546-v2.pdf
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9196144/