Rezistența la insulină se manifestă cu o reducere a absorbției și oxidării glucozei și reduceri ale sintezei glicogenului și capacitatea de a suprima oxidarea lipidelor. Prin afectarea căii insulinei PI3-K, rezistența la insulină joacă un rol cheie în dezvoltarea disfuncției metabolice și stă la baza unui grup de anomalii cardiovasculare și metabolice denumite sindrom metabolic (inclusiv hipertensiune arterială, dislipidemie și disglicemie).
Mai mult, rezistența la insulină promovează creșterea în greutate legată de hiperinsulinemia compensatorie secundară, rezultând un cerc vicios de agravare a rezistenței la insulină și a efectelor sale metabolice.
Ce este sindromul metabolic?
Sindromul metabolic, cunoscut și sub numele de sindromul X, este o afecțiune medicală complexă și multifactorială, caracterizată prin prezența a cel puțin trei dintre următoarele condiții: obezitate abdominală, nivel ridicat al trigliceridelor, nivel scăzut al colesterolului HDL, hipertensiune arterială și nivel crescut al glucozei în sânge.
Hai să vedem care sunt valorile de la care ar trebui să investigăm ce se întâmplă cu corpul nostru:
- Obezitate abdominală – aceasta se stabilește în funcție de circumferința taliei: valori mai mari de 85 cm la femei și 94 cm la bărbați semanlizează obezitatea.
- Trigliceridele – un nivel mai mare de 150 mg/dL este considerat ridicat.
- Colesterolul HDL – un nivel mai mic de 40 mg/dL la bărbați și 50 mg/dL la femei este considerat scăzut.
- Tensiunea arterială – valori de 130/80 mm Hg sau mai mari sunt considerate cu risc de obezitate. De asemenea, hipertensiunea arterială este asociată cu rezistența la insulină.
- Nivelul glucozei în sânge – o valoare mai mare sau egală cu 100 mg/dL semnalizează un risc crescut de sindrom metabolic.
Clasificarea sindromului metabolic se bazează pe criteriile stabilite de Organizația Mondială a Sănătății (OMS) și de Federația Internațională de Diabet, având o prevalenţă ridicată în întreaga lume. Se estimează că 20-25% din populaţia planetei prezintă această afecţiune.
În plus, persoanele cu sindrom metabolic au un risc de cinci ori mai mare de a dezvolta diabet de tip 2. S-ar adăuga celor 230 de milioane de oameni din întreaga lume care au deja diabet, una dintre cele mai frecvente boli cronice la nivel mondial și a patra sau a cincea cauză principală de moartea în lumea dezvoltată. Gruparea factorilor de risc pentru bolile cardiovasculare (BCV) care caracterizează sindromul metabolic este acum considerată a fi forța motrice pentru o nouă epidemie de BCV.
Care sunt simptomele sindromului metabolic?
Nu toate aspectele sindromului metabolic provoacă simptome. Deci, simptomele vor varia în funcție de ce afecțiune ai. De exemplu, tensiunea arterială ridicată, trigliceridele mari și colesterolul HDL scăzut, de obicei, nu provoacă simptome.
Nivelul ridicat de zahăr din sânge (hiperglicemia) poate provoca simptome pentru unele persoane, cum ar fi:
- pielea întunecată de la axile sau din spatele și părțile laterale ale gâtului (acanthosis nigricans).
- vedere în ceață.
- sete crescută (polidipsie).
- urinare frecventă, mai ales noaptea.
- oboseală.
Ce cauzează sindromul metabolic?
Patogeneza unui sindrom metabolic implică o serie de mecanisme complexe care sunt încă în curs de cercetare și dezbatere, în comunitatea științifică, dar atât rezistența la insulină, cât și obezitatea centrală sunt considerați factori importanți. Genetica, inactivitatea fizică, îmbătrânirea, o stare proinflamatoare și modificările hormonale pot avea, de asemenea, un efect cauzal, dar rolul acestora poate varia în funcție de grupul etnic.
Rezistența la insulină apare atunci când celulele din organism (ficatul, mușchiul scheletic și țesutul adipos/gras) devin mai puțin sensibile și în cele din urmă rezistente la insulină, hormonul care este produs de celulele beta din pancreas pentru a facilita absorbția glucozei. Glucoza nu mai poate fi absorbită de celule, ci rămâne în sânge, declanșând nevoia de a produce din ce în ce mai multă insulină (hiperinsulinemie) în încercarea de a procesa glucoza.
Producția de cantități din ce în ce mai mari de insulină slăbește și poate uza în cele din urmă celulele beta.
Odată ce pancreasul nu mai este capabil să producă suficientă insulină, atunci o persoană devine hiperglicemică (prea multă glucoză în sânge) și va fi diagnosticată cu diabet de tip 2.
Chiar înainte de a se întâmpla acest lucru, organismul suferă daune majore, inclusiv o acumulare de trigliceride care afectează și mai mult sensibilitatea la insulină.
Obezitatea este asociată cu rezistența la insulină și cu sindromul metabolic. Obezitatea contribuie la hipertensiune arterială, colesterol seric ridicat, HDL scăzut și hiperglicemie și este asociată independent cu un risc mai mare de BCV. Riscul de consecințe grave asupra sănătății sub forma diabetului de tip 2, bolilor coronariene (CHD) și o serie de alte afecțiuni, inclusiv unele forme de cancer, s-a dovedit a crește odată cu creșterea indicelui de masă corporală (IMC). De asemenea, un exces de grăsime corporală în zona abdomenului (circumferința taliei adică) este un indicator mai bun al sindromului metabolic decât IMC. International Obesity Task Force (IOTF) raportează că 1,7 miliarde din populația lumii este deja expusă unui risc crescut de boli netransmisibile legate de greutate, cum ar fi diabetul de tip 2.
Rolul rezistenței la insulină în dezvoltarea sindromului metabolic
În continuare vom oferi o privire de ansamblu asupra mecanismelor prin care rezistența la insulină contribuie la disfuncția metabolică.
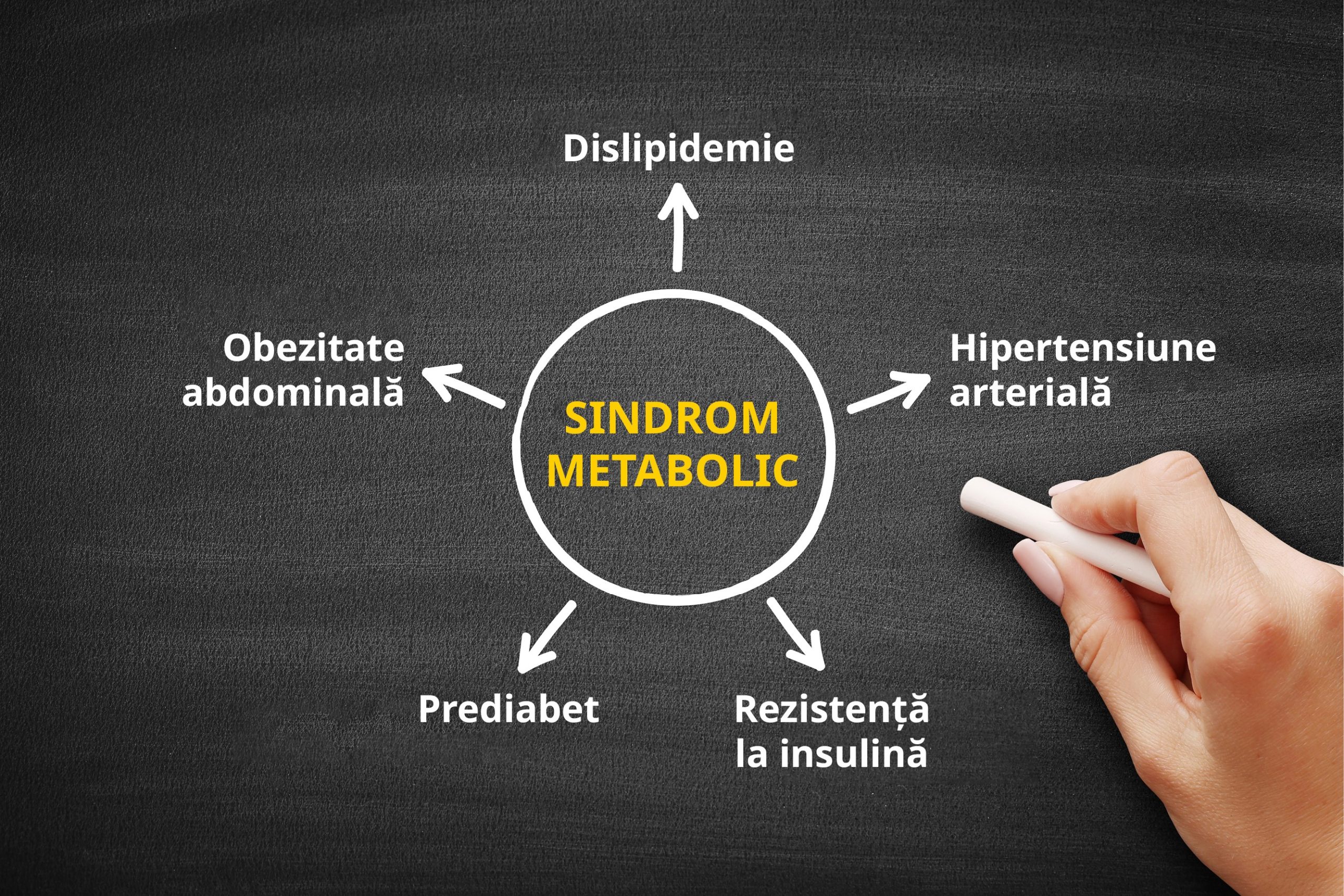
Hipertensiune arterială: rezistența la insulină duce la hiperinsulinemie compensatorie care, la rândul său, poate crește tensiunea arterială prin mecanisme multiple. Acestea includ reabsorbția renală îmbunătățită a sodiului, hipertrofia vaselor de sânge de rezistență și activarea sistemului nervos simpatic. Dezvoltarea hipertensiunii poate duce, de asemenea, la agravarea rezistenței la insulină prin modificări ale structurii vasculaturii și afectarea vasodilatației în mușchii scheletici, cu livrarea redusă de glucoză și insulină către celulele musculare scheletice. Interesant, totuși, studiile pe modele animale de hipertensiune sugerează că rezistența la insulină precede de fapt debutul hipertensiunii, în concordanță cu rolul cauzal al rezistenței la insulină în dezvoltarea hipertensiunii. Mai mult, datele de la voluntari umani sănătoși sugerează că schimbările în reglarea autonomă influențează sensibilitatea la insulină. Prin urmare, dezechilibrul autonom poate avea ca rezultat atât rezistența la insulină, cât și hipertensiune arterială, prin efecte asupra vasoconstricției.
Dislipidemie: rezistența la insulină are ca rezultat creșterea fluxului hepatic de acizi grași proveniți din dietă și rezistență la efectele antilipolitice ale insulinei în țesutul adipos.
Aceste modificări ale metabolismului lipidic se manifestă prin dislipidemie și o triadă lipidică proaterogenă caracteristică constând în niveluri plasmatice ridicate de trigliceride, lipoproteine mici și dense de joasă densitate și niveluri plasmatice scăzute de lipoproteine cu densitate mare. În plus, astfel de modificări ale profilului lipidic induse de rezistența la insulină pot contribui la răspunsuri inflamatorii în endoteliu.
Disglicemie: rezistența la insulină se asociază cu un metabolism dezechilibrat al glucozei și cu hiperglicemie cronică care, la rândul lor, pot declanșa stres oxidativ și un răspuns inflamator. Reducerea absorbției periferice a glucozei în celulele musculare scheletice reprezintă o caracteristică cardinală a rezistenței la insulină. În acest context, hiperinsulinemia compensatorie datorată eliberării sporite de insulină din celulele β pancreatice ajută la atenuarea dezvoltării hiperglicemiei. Prin urmare, dezvoltarea diabetului zaharat de tip 2 necesită în plus un grad de disfuncție a celulelor β pancreatice.
Interesant este că datele din studiile fiziologice și epidemiologice sugerează că secreția dezordonată de insulină din celulele β pancreatice poate contribui de fapt la dezvoltarea rezistenței la insulină și a diabetului zaharat de tip 2 ulterioare.
Consecințele metabolice ale rezistenței la insulină coexistă adesea și contribuie împreună la disfuncția endotelială și, în cele din urmă, la formarea plăcii aterosclerotice. Aceste procese patogene se pot manifesta în cele din urmă cu evenimente macrovasculare. În cazul miocardului, rezistența la insulină provoacă, de asemenea, leziuni prin mai multe căi care includ livrarea modificată a substraturilor, inclusiv acizii grași liberi, reglarea afectată a metabolismului substratului și alterarea transducției semnalului.
În plus, rezistența la insulină ca factor patogen primar stă la baza bolii hepatice grase nonalcoolice.
În sfârșit, rezistența la insulină probabil joacă un rol cheie în patogenia complexă care stă la baza sindromului de ovar polichistic prin disfuncția metabolică care provine din rezistența la insulină selectivă în cadrul căii postreceptoare a insulinei PI3-K și efectele dăunătoare ale hiperinsulinemiei compensatorii asupra funcției ovariene.
Reversibilitatea rezistenței la insulină cu intervenții în stilul de viață
Deși rezistența la insulină joacă un rol central în patogeneza complexă a disfuncției metabolice și a disfuncției cognitive la persoanele care se îngrașă și dezvoltă obezitate, date convingătoare susțin un efect important al factorilor stilului de viață asupra sensibilității la insulină. Fără îndoială, unele dintre îmbunătățirile sensibilității la insulină ca urmare a adoptării factorilor unui stil de viață sănătos provin din pierderea în greutate asociată și reducerea excesului de țesut adipos.
Dovezile actuale promovează o atenție sporită pentru optimizarea stilului de viață în gestionarea eficientă a rezistenței la insulină legată de obezitate, ca mijloc de îmbunătățire a riscului cardiovascular viitor și a stării de sănătate generale.

Cei 3 piloni principali ai stilului de viață care ajută în managementul rezistenței la insulină sunt:
- Activitatea fizică: Multe dovezi susțin rolul important pe care îl are activitatea fizică regulată în optimizarea sensibilității la insulină și efectele negative ale sedentarismului asupra rezistenței la insulină. Antrenamentul acționează asupra sensibilitatii la insulina prin optimizarea transportului si metabolismului glucozei
- Dieta: În ceea ce privește efectele nutrienților asupra sensibilității la insulină, cele mai multe și convingătoare dovezi se referă la aportul de fibre alimentare. De asemenea, dietele cu conținut scăzut de carbohidrați sau cu indice glicemic scăzut sunt asociate cu îmbunătățiri mai mari, atât ale profilului rezistenței la insulină, cât și al lipidelor. Prin urmare, poate cea mai bună opțiune a noastră este să asigurăm combinația dintre o dietă bogată în fibre și săracă în carbohidrați.
- Somnul: Este o componentă esențială a fiziologiei umane. Din păcate, lipsa de somn a devenit comună în societatea noastră modernă. Privarea de somn are implicații de amploare care se extind cu mult dincolo de rezistența la insulină și disfuncția metabolică. În ultimii ani, au apărut o mulțime de date care oferă dovezi clare pentru a lega privarea de somn cu un risc crescut de rezistență la insulină, obezitate și diabetul zahar de tip 2.
Prevenție înainte de toate!
Cel mai bun mod de a preveni sindromul metabolic, de a-l trata și de a preveni complicațiile este printr-un stil de viață sănătos.
Așa DA
- încearcă să slăbești dacă ești supraponderal.
- mănâncă mai puține grăsimi saturate, carne și produse lactate, și consumă mai multe fructe, legume și cereale integrale.
- fă cel puțin 150 de minute de exerciții fizice moderate până la intense pe săptămână, repartizate pe cel puțin 4 sau 5 zile.
Așa NU
- statul la birou pentru perioade lungi de timp, fără pauze.
- dietă dezechilibrată, bogată în alimente procesate și zahăr.
RESURSE
https://idf.org/media/uploads/2023/05/attachments-30.pdf
https://publications.aston.ac.uk/id/eprint/42233/1/ijms-22-00546-v2.pdf
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4129661/
https://my.clevelandclinic.org/health/diseases/10783-metabolic-syndrome